题目内容
13.书写下列方程式(1)不用铁桶盛放硫酸铜溶液的原因Fe+CuSO4=FeSO4+Cu.
(2)高炉炼铁的原理Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)酒精燃烧的方程式2C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,不用铁桶盛放硫酸铜溶液,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu;
(2)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式
为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(写其他铁的氧化物对应的反应也可以)
(3)酒精和氧气在点燃的条件下生成水和二氧化碳,化学方程式为:2C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
故答案为:(1)Fe+CuSO4=FeSO4+Cu;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)2C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
9.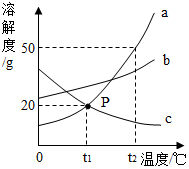 如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
 如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )| A. | t1℃时,a、c两种物质的饱和溶液中溶质质量一定相等 | |
| B. | t2℃时,将50g a物质放入50g水中充分溶解后只能得到75g a的饱和溶液 | |
| C. | 将t1℃时a、b、c三种物质的饱和溶液升温至t2℃时,所得溶液的溶质质量分数关系是b>a>c | |
| D. | c的饱和溶液降温后,溶质质量分数保持不变 |
8.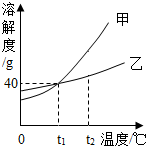 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g | |
| C. | t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 | |
| D. | t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙 |
18.实验结束后,如图仪器的放置方法正确的是( )
| A. |  | B. |  | ||
| C. | 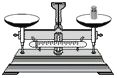 | D. | 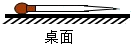 |
 已知A、E、F是单质,B、C、D是 化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成,其中B是相对分子质量最小的氧化物,D物质很不稳定,常温下就容易分解生成B和C,它们之间的转化关系如图所示,请据图完成下列内容:
已知A、E、F是单质,B、C、D是 化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成,其中B是相对分子质量最小的氧化物,D物质很不稳定,常温下就容易分解生成B和C,它们之间的转化关系如图所示,请据图完成下列内容: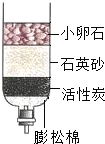 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.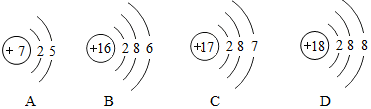 碘元素(元素符号为I)的原子结构示意图为
碘元素(元素符号为I)的原子结构示意图为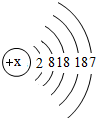 ,请回答下列问题.
,请回答下列问题.