题目内容
在实验室里加热30g氯酸钾(KClO3)和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g。请计算:
(1)生成氧气的质量为 g; (2)原混合物中氯酸钾的质量。
【答案】
(1)9.6g
(2)24.5g
【解析】
试题分析:(1)该反应中,反应物是氯酸钾,生成物是氯化钾和氧气,二氧化锰是催化剂,反应前后质量不变。根据质量守恒定律,化学反应前后物质的总质量不变,氧气是气体会逸散到空气中,所以减少的质量就为氧气的质量。氧气的质量=30g - 20.4g=9.6g
(2)利用化学方程式中氯酸钾与氧气的质量比,结合氧气的质量,可求出原混合物中氯酸钾的质量
解:设原混合物中氯酸钾的质量为x
2KClO3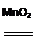 2KCl
+ 3O2 ↑
2KCl
+ 3O2 ↑
245 96
X 9.6g
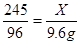 x=24.5g
x=24.5g
答:原混合物中氯酸钾的质量的为24.5g。
考点:根据化学反应方程式的计算

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 量。
量。