题目内容
4.下列物质肯定为纯净物的是( )| A. | 由同种元素组成的物质 | |
| B. | 由不同种元素组成的物质 | |
| C. | 由不同种分子构成的物质 | |
| D. | 由一种阳离子和另一种的阴离子构成的物质 |
分析 根据纯净物的定义和组成特点分析,纯净物是由一种物质组成的.
解答 解:A、由同种元素组成的物质,不一定是纯净物,例如,石墨与金刚石混合在一起,由碳元素组成,属于混合物,所以,A错误;
B、由不同种元素组成的物质,不一定是纯净物,例如,空气中含有多种元素,属于混合物,所以,B错误;
C、由不同种分子构成的物质,物质的组成种类不只有一种,属于混合物物,所以,C错误;
D、由一种阳离子和另一种的阴离子构成的物质,是离子化合物,属于纯净物,D正确.
故选D.
点评 本题主要考查了纯净物的概念,解答时要分析物质的组成,如果只有一种物质组成就属于纯净物,如果有多种物质组成就属于混合物.

练习册系列答案
相关题目
15.含碳元素的物质广泛存在,请回答下列问题:
(1)根据如图提供的信息,在相应的位置上填写出不同碳单质的名称或化学式:
(2)一氧化碳和二氧化碳都是碳的氧化物,却有不同的化学性质,试举例说明:一氧化碳具有可燃性,二氧化碳不能燃烧;请从微观角度分析它们性质不同的原因:构成它们的分子不同;
(3)二氧化碳与人类生命活动密切相关,大气中的二氧化碳溶于水可形成碳酸,有关的化学方程式是CO2+H2O═H2CO3,植物的光合作用离不开二氧化碳,有关反应可表示为:CO2+H2O $→_{叶绿素}^{光}$淀粉+O2.以上两个反应的反应物相同但产物却不同,说明化学反应的产物不仅决定于反应物,还决定于反应条件.
(4)近几十年来,大气中CO2的含量不断上升,使全球变暖.导致大气中CO2含量不断上升的主要因素是(填写序号)③.
①人和动物的呼吸 ②植物的光合作用 ③化石燃料的大量使用和森林遭到破坏.
(1)根据如图提供的信息,在相应的位置上填写出不同碳单质的名称或化学式:
 |  |  |
| 名称:石墨 | 化学式:C60 | 名称:金刚石 |
(3)二氧化碳与人类生命活动密切相关,大气中的二氧化碳溶于水可形成碳酸,有关的化学方程式是CO2+H2O═H2CO3,植物的光合作用离不开二氧化碳,有关反应可表示为:CO2+H2O $→_{叶绿素}^{光}$淀粉+O2.以上两个反应的反应物相同但产物却不同,说明化学反应的产物不仅决定于反应物,还决定于反应条件.
(4)近几十年来,大气中CO2的含量不断上升,使全球变暖.导致大气中CO2含量不断上升的主要因素是(填写序号)③.
①人和动物的呼吸 ②植物的光合作用 ③化石燃料的大量使用和森林遭到破坏.
12.取三种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁,各取少许花汁,用稀盐酸和稀碱进行检验,结果如表所示:
则下列说法不正确的是( )
| 花的种类 | 花汁在酒精中的颜色 | 花汁在酸溶液中的颜色 | 花汁在碱溶液中的颜色 |
| 大红花 | 粉红色 | 橙色 | 绿色 |
| 万寿菊 | 黄色 | 黄色 | 黄色 |
| 雏菊 | 无色 | 无色 | 黄色 |
| A. | 研磨花瓣时加入酒精是为了溶解其中的色素 | |
| B. | 万寿菊不能用作酸碱指示剂 | |
| C. | 遇到pH=10的溶液,大红花汁会变成粉红色 | |
| D. | 可用雏菊花汁来区别稀盐酸和氢氧化钠溶液 |
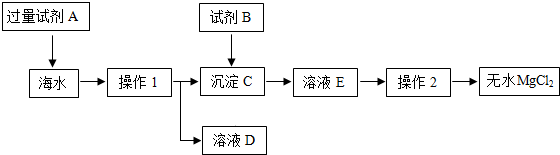
19.海水主要含有NaCl、MgCl2等物质,目前世界上60%的镁是从海水中提取的.小红同学模拟如图化工厂生产流程,以海水和贝壳(主要成分是碳酸钙)为原料来制取生产镁的原料----无水MgCl2.
(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
(2)除杂过程
请回答:
①在30℃,试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g的Mg.

(1)查阅资料.
氢氧化钠和氢氧化钙两种物质溶解度随温度变化表
| 温度(℃) 溶解度(g) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 氢氧化钠 | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | 314 | 329 |
| 氢氧化钙 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 | 0.105 | 0.095 | 0.08 |
请回答:
①在30℃,试剂A最好选用:NaOH(填化学式).在海水中加入试剂A时发生反应的化学方程式是MgCl2+2NaOH=Mg(OH)2↓+2NaCl.
②若在实验室进行操作1,需要用到的玻璃仪器除漏斗、玻璃棒外,还有烧杯.
③试剂B与沉淀C发生反应的化学方程式是Mg(OH)2+2HCl=MgCl2+2H2O.
④MgCl2的相对分子质量是95,47.5g的MgCl2中含有12g的Mg.
9.继“食盐加碘”之后,我国又将启动“酱油加铁”,其意义在于:( )
①补充人体需要的铁元素
②预防缺铁性贫血
③改善酱油的味道增加黑色素
④减少厨房污染物,提高人们的健康水平.
①补充人体需要的铁元素
②预防缺铁性贫血
③改善酱油的味道增加黑色素
④减少厨房污染物,提高人们的健康水平.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ①②④ |
16.一定质量的硫酸溶液,用40克质量分数为20%的氢氧化钠溶液恰好中和,现改用40克质量分数为20%的氢氧化钾溶液,当完全反应后,滴加紫色石蕊试液,则( )
| A. | 试液变红 | B. | 试液变蓝 | C. | 试液不变色 | D. | 无法确定 |
13. “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.
【提出问题】:久置固体的成分是什么?
【收集资料】:
1、查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
2、打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体.
【作出猜想】:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【实验探究】:如表是甲组同学涉及并记录的实验报告,请你补充完整.
【实验质疑】:乙组同学认为甲组同学在实验中得出“一定不含有Fe2O3”的结论是错误的,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色;你认为甲组同学哪一步操作得出的结论也不合理操作二,理由是(用化学方程式表示)CaO+H2O=Ca(OH)2.
【继续探究】:为验证固体中是否含有Fe2O3,乙组同学用磁铁先分离出铁粉,向残留固体中加入足量稀盐酸,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式Fe2O3+6HCl=2FeCl3+3H2O.
 “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,涉及实验进行探究.【提出问题】:久置固体的成分是什么?
【收集资料】:
1、查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
2、打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体.
【作出猜想】:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【实验探究】:如表是甲组同学涉及并记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| 一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有CaO. |
| 二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
| 三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有Fe,一定不含有Fe2O3 |
| 四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3. |
【继续探究】:为验证固体中是否含有Fe2O3,乙组同学用磁铁先分离出铁粉,向残留固体中加入足量稀盐酸,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式Fe2O3+6HCl=2FeCl3+3H2O.
 某补钙剂说明书的部分信息如图所示,现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g.
某补钙剂说明书的部分信息如图所示,现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g.