题目内容
4.分别选用一种物质除去下列物质中的杂质,括号内为杂质.(1)二氧化碳(一氧化碳)将混合气体通过灼热的氧化铜;
(2)白糖(细沙)加水溶解、过滤、蒸发.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)根据一氧化碳和二氧化碳的化学性质,一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不与氧化铜不反应,故可将混合气体通过灼热的氧化铜.
(2)白糖易溶于水,细沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂.
故答案为:(1)将混合气体通过灼热的氧化铜;(2)加水溶解、过滤、蒸发.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.下列说法不正确的是( )
| A. | 二氧比钛属于氧化物 | |
| B. | 萘胺由三种元素组成 | |
| C. | 萘胺中氮元素的质量分数约为11.9% | |
| D. | 萘胺中碳、氢、氮三种元素的质量之比为120:9:14 |
19.下列化学反应中属于分解反应的是( )
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 |
9.如表是某指示剂在一定pH范围内显示的颜色,向滴有少量该指示剂的氢氧化钠溶液中,加入稀硫酸,出现的颜色变化可能是( )
| 颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
| pH范围 | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
| A. | 由红变紫 | B. | 由蓝变绿 | C. | 由绿变橙 | D. | 由蓝变紫 |
16.下列有关微观粒子的说法中正确的是( )
| A. | 分子是由原子构成的 | |
| B. | 物质都是由离子构成的 | |
| C. | 原子中的粒子都不带电 | |
| D. | 分子是保持物质化学性质的唯一粒子 |
10.有化合价升降的反应是氧化还原反应,下列一定不是氧化还原反应的是( )
| A. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | Cl2+2NaI═2NaCl+I2 | D. | CO2+H2O═H2CO3 |
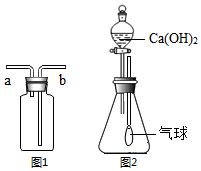 根据图1、图2回答下列问题:
根据图1、图2回答下列问题: