题目内容
14. 干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质$?_{反映}^{决定}$物质用途”这一角度分析干冰具有的性质和用途.
干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质$?_{反映}^{决定}$物质用途”这一角度分析干冰具有的性质和用途.(1)干冰升华时吸收(填“吸收”或“放出”)大量热,因此可作制冷剂或用于人工降雨.
(2)干冰转化成二氧化碳气体后,能参与绿色植物的光合作用,故在大棚蔬菜种植中作气体肥料.
(3)试写一条二氧化碳的用途二氧化碳不能燃烧,也不支持燃烧,密度又比空气大,故可以用来灭火.
分析 物质的性质决定了物质的用途.二氧化碳能溶于水,可用来生产碳酸饮料、啤酒、汽水;二氧化碳的固体俗你干冰升华时吸收大量的热,可用作致冷剂;二氧化碳不能燃烧也不支持燃烧密度大于空气,可用于灭火;二氧化碳不维持呼吸,仓库里常充入二氧化碳,防止粮食虫蛀和蔬菜腐烂,延长保存期.等等
解答 解:(1)致冷剂用来使周围温度降低,干冰升华吸收大量热,使周围温度降低.
故答案为:吸收;
(2)二氧化碳是光合作用的主要原料,增加空气中二氧化碳含量可加快光合作用,温室大棚常把二氧化碳当作肥料.
故答案为:气体肥料;
(3)二氧化碳不能燃烧,也不支持燃烧,密度又比空气大,故可以用来灭火(或二氧化碳溶于水,可制汽水等碳酸饮料或啤酒等;或二氧化碳溶于水制成碳酸水,可改良碱性土壤;或二氧化碳能与氢氧化钙反应,使石灰浆刷的墙面变坚硬;二氧化碳是光合作用的原料,温室里直接施用二氧化碳作肥料,可以增进植物的光合作用,促进农作物生长,增加产量)
故答案为:二氧化碳不能燃烧,也不支持燃烧,密度又比空气大,故可以用来灭火.
点评 物质的性质决定物质的用途,物质的用途反过来反映出物质的性质.把物质性质与用途结合起来,可以更好地记住物质的用途,也能更深地理解物质的性质.

练习册系列答案
相关题目
4.下列变化中与其他变化本质不同的是( )
| A. | 石油的分馏 | B. | 煤的气化 | C. | 煤的焦化 | D. | 煤的液化 |
2.石灰石的主要成分是碳酸钙,某实验课上同学们对碳酸钙高温加热一段时间剩余固体的成分进行了探究.
【提出问题】剩余固体成分是什么?
【猜想与假设】
A.全部是碳酸钙 B.全部是氧化钙 C.碳酸钙和氧化钙的混合物
【设计并完成实验】请填写(1)中结论和(2)中的实验步骤及实验现象
【实验结论】通过以上实验得出,原A、B、C三个假设中,假设C(填字母)成立.
【讨论交流】有同学提出证明实验(1)的结论可用“取少量固体于试管中,加适量水振荡,直接通入CO2,看溶液是否变浑浊”的方案也行.你是否赞成他的观点,不赞成,原因是CaO 与水反应生成的Ca(OH)2微溶于水,溶液变浑浊不能说明是CO2与Ca(OH)2反应的产物所致.
【提出问题】剩余固体成分是什么?
【猜想与假设】
A.全部是碳酸钙 B.全部是氧化钙 C.碳酸钙和氧化钙的混合物
【设计并完成实验】请填写(1)中结论和(2)中的实验步骤及实验现象
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液. | 溶液变红 | 剩余固体成分中一定含有CaO(填化学式) |
| (2)取少量固体于试管中,加适量稀盐酸,观察现象, | 有大量气泡产生 | 剩余固体成分中一定含有碳酸钙 |
【讨论交流】有同学提出证明实验(1)的结论可用“取少量固体于试管中,加适量水振荡,直接通入CO2,看溶液是否变浑浊”的方案也行.你是否赞成他的观点,不赞成,原因是CaO 与水反应生成的Ca(OH)2微溶于水,溶液变浑浊不能说明是CO2与Ca(OH)2反应的产物所致.
4.下列两种物质相互混合后,不会发生反应的是( )
| A. | 碳酸钠溶液和氯化钡溶液 | B. | 氢氧化钠溶液和硝酸钡溶液 | ||
| C. | 氢氧化钙溶液和氯化铁溶液 | D. | 盐酸和硝酸银溶液 |

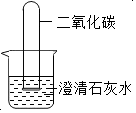 如图所示,将一个充满二氧化碳的试管倒插入装有澄清石灰水的烧杯里,可观察的现象是澄清石灰水变浑浊、试管内液面上升.
如图所示,将一个充满二氧化碳的试管倒插入装有澄清石灰水的烧杯里,可观察的现象是澄清石灰水变浑浊、试管内液面上升.