题目内容
①、②、③、④四个烧杯分别盛有50g水,在20℃时,向四个烧杯中依次加入27g、9g、36g、18g的NaCl,充分溶解后的情况如图所示,则下列叙述不正确的是( )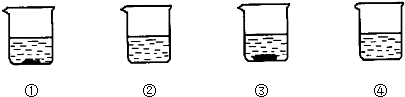

| A、①③溶液的溶质质量分数不一定相等 | B、②中所得溶液一定是最稀的溶液 | C、④所得溶液的溶质质量分数为36% | D、如果①②中的物质混合后全部溶解,则其与④中溶液溶质质量分数一定相同 |
分析:根据在一定温度和溶剂中,有溶质析出的溶液中,溶质达到最大溶解能力,溶质不会溶解,则溶液一定为饱和溶液,没有固体析出的溶液可能是恰好饱和或不是饱和溶液;在饱和溶液中溶质的质量分数最大且相同进行解答.
解答:解:依据饱和溶液的概念可知,①、③中有固体出现,一定是饱和溶液,④中的溶质质量比②多,而比①的少,可能是恰好溶解,则可能饱和,②一定不饱和溶液.
A、①、③溶液都是饱和溶液,所以溶液的溶质质量分数一定相等,故A错误;
B、②中所得溶液中溶解的溶质最少,所以一定是最稀的溶液,故B正确;
C、④所得溶液的溶质质量分数为
×100%=26.5%,故C错误;
D、①②中的物质混合后全部溶解,所得溶液的溶质质量分数=
×100%=26.5%,④所得溶液的溶质质量分数为
×100%=26.5%,故D正确.
故选:AC.
A、①、③溶液都是饱和溶液,所以溶液的溶质质量分数一定相等,故A错误;
B、②中所得溶液中溶解的溶质最少,所以一定是最稀的溶液,故B正确;
C、④所得溶液的溶质质量分数为
| 18g |
| 50g+18g |
D、①②中的物质混合后全部溶解,所得溶液的溶质质量分数=
| 27g+9g |
| 50g+50g+27g+9g |
| 18g |
| 50g+18g |
故选:AC.
点评:本题考查了学生对饱和溶液的判断及饱和溶液与不饱和溶液的转化,应注意条件的变化来分析解答.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
某校兴趣小组探究学校附近赤铁矿中Fe2O3的纯度.他们采集了80g矿样,粉碎后均分成四等份,分别置于四个烧杯中,然后分别向四个烧杯中加入同一浓度的稀硫酸,加入硫酸的质量与反应后剩余固体质量如下表所示.(假设矿石中的杂质既不和稀硫酸反应,也不溶于水)
求:
(1)该矿样中Fe2O3的质量分数.
(2)所用稀硫酸的溶质质量分数.
| 实验1 | 实验2 | 实验3 | 实验4 | |
| 加稀硫酸质量 | 150g | 240g | 330g | 400g |
| 剩余固体质量 | 12g | 7.2g | 4g | 4g |
(1)该矿样中Fe2O3的质量分数.
(2)所用稀硫酸的溶质质量分数.

 B、
B、 C、
C、 D、
D、