题目内容
2.金属材料被广泛应用于我们的生活,不仅是因为其物理性能优良,还与它们的化学性质密切相关.下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究.【实验目的】测定金属铁、铜和镁的活动性强弱.
【所用试剂】稀硫酸,硝酸银溶液,光亮的薄铁片、薄铜片、薄镁片.
【实验过程】
步骤Ⅰ:将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧的现象;
步骤Ⅱ:将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的稀硫酸的试管中;
步骤Ⅲ:将铁片、铜片、镁片分别放入三只盛有溶质质量分数相同、体积相同的硝酸银溶液的试管中.
实验现象记录表
| 金属 | 空气 | 稀硫酸 | 硝酸银溶液 |
| 铁 | - | √ | √ |
| 铜 | - | - | √ |
| 镁 | √ | √ | √ |
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是镁能够在空气中燃烧.
(2)运用“控制变量法”设计实验方案是化学研究的重要方法.步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是温度.
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是Mg>Fe>Cu(元素符号表示).
【反思与交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是镁和稀硫酸反应的速率太快,不利于控制和收集.
分析 镁比铁活泼,铁比铜活泼;
实验室制取气体选择药品时,要考虑反应速率、药品价格、环境污染、操作是否简单易行等.
解答 解:(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是镁能够在空气中燃烧.
故填:镁;镁能够在空气中燃烧.
(2)步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶质质量分数以外,还需要控制的条件是温度,这是因为温度是影响反应速率的一个重要因素.
故填:温度.
【实验结论】通过步骤Ⅰ可以得出镁最活泼,通过表中信息可知铁比铜活泼,因此金属铁、铜和镁的活动性由强到弱的顺序是Mg>Fe>Cu.
故填:Mg>Fe>Cu.
【反思与交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是镁和稀硫酸反应的速率太快,不利于控制和收集.
故填:镁和稀硫酸反应的速率太快,不利于控制和收集.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
12.下列有关溶液的说法正确的是( )
| A. | 浓溶液的质量分数一定比稀溶液的质量分数高 | |
| B. | 同种溶质的饱和溶液一定比它的不饱和溶液的质量分数大 | |
| C. | 饱和溶液转化为不饱和溶液溶液的质量一定增大 | |
| D. | 饱和溶液恒温蒸发部分溶剂后溶质的质量分数一定不变 |
10.《三国演义》中有这样一个故事:诸葛亮率领的汉军误饮了“哑泉”.“哑泉,人若饮之,则不能言,不过旬晶必死”.后来,汉军将士经地方隐士指点,饮了万安溪的“安乐泉”水方才转危为安.“哑泉”和“安乐泉”中所含的化学物质可能分别是( )
| A. | NaCl、CaCl2 | B. | Na2SO4、BaCl2 | C. | FeCl3、NaOH | D. | CuSO4、Ca(OH)2 |
17.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 碳酸钠溶液和稀盐酸反应Na2CO3+2HCl--NaCl+H2O+CO2复分解反应 | |
| B. | 用过氧化氢溶液和二氧化锰制氧气 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ 分解反应 | |
| C. | 用铁制容器盛放稀盐酸 2Fe+6HCl--2FeCl2+3H2↑置换反应 | |
| D. | 用熟石灰制生石灰 CaO+H2O--Ca(OH)2化合反应 |
7.“遥知不是雪,为有暗香来”说明( )
| A. | 分子之间有间隔 | B. | 分子不断运动 | C. | 分子很小 | D. | 分子可分 |
14.如图是几种粒子的结构示意图,有关说法正确的是( )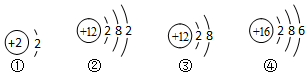
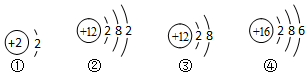
| A. | 只有①达到了稳定结构 | B. | ①②元素具有相似的化学性质 | ||
| C. | ②失去电子以后形成的是阳离子 | D. | ④属于金属元素 |
11.某化学小组为了探究一瓶久置在空气中的氢氧化钠样品(不含有水分)的变质程度,进行了如下实验:取该氢氧化钠样品13.3g于烧杯中,加水完全溶解,然后向烧杯中逐渐加入一定溶质质量分数的氯化钡溶液,反应过程中对加入氯化钡溶液的质量与烧杯中产生沉淀的质量进行了记录,部分数据见表.
试分析计算:
(1)13.3g氢氧化钠样品中碳酸钠的质量;
(2)13.3g氢氧化钠样品变质前的质量.(已知:Ba的相对原子质量为137)
| 加入氯化钡溶液的质量/g | 20 | 40 | 80 |
| 生成沉淀的质量/g | 1.97 | 3.94 | 5.91 |
(1)13.3g氢氧化钠样品中碳酸钠的质量;
(2)13.3g氢氧化钠样品变质前的质量.(已知:Ba的相对原子质量为137)