题目内容
氢氧化钠是一种重要的化工基础原料,广泛地应用于造纸、纺织、石油化工、印染等行业.
(1)氢氧化钠的俗名是 (只写一种).氢氧化钠与硫酸反应的化学方程式为 .
(2)实验室有一瓶久置的固体,标签上写着“氢氧化钠”.为了检验里面是否还存在NaOH,实验员取少量该固体样品进行以下实验: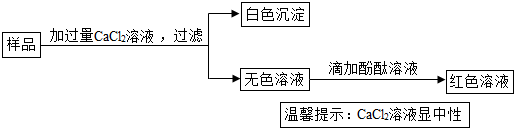
①根据溶液变红这一现象说明样品中含有 (填序号).
A.CaCl2 B.Na2CO3 C.NaOH D.Na2CO3和NaOH
②用化学方程式表示氢氧化钠变质的原因 ;
③在实验室里氢氧化钠需要密封保存,药品密封保存的原因很多,请你写出浓盐酸需要密封保存的原因 .
(1)氢氧化钠的俗名是
(2)实验室有一瓶久置的固体,标签上写着“氢氧化钠”.为了检验里面是否还存在NaOH,实验员取少量该固体样品进行以下实验:

①根据溶液变红这一现象说明样品中含有
A.CaCl2 B.Na2CO3 C.NaOH D.Na2CO3和NaOH
②用化学方程式表示氢氧化钠变质的原因
③在实验室里氢氧化钠需要密封保存,药品密封保存的原因很多,请你写出浓盐酸需要密封保存的原因
考点:碱的化学性质,常见碱的特性和用途,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)根据氢氧化钠的俗称为烧碱、火碱、苛性钠进行分析;根据氢氧化钠与硫酸反应生成硫酸钠和水正确书写化学方程式;
(2)
①根据氢氧化钠显碱性可使酚酞试液变红进行分析回答;
②根据氢氧化钠能与二氧化碳反应生成碳酸钠和水而变质解答;
③根据浓盐酸的特性解答.
(2)
①根据氢氧化钠显碱性可使酚酞试液变红进行分析回答;
②根据氢氧化钠能与二氧化碳反应生成碳酸钠和水而变质解答;
③根据浓盐酸的特性解答.
解答:解:
(1)氢氧化钠俗称为:烧碱、火碱、苛性钠等.氢氧化钠与硫酸反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O;
(2)
①滴加酚酞试液溶液变红,说明溶液显碱性,故含有氢氧化钠,碳酸钠虽然也显碱性,但由于加入了过量的氯化钙,所以溶液中无碳酸钠,故选C;
②氢氧化钠易与二氧化碳反应生成碳酸钠而变质,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
③浓盐酸具有挥发性,会导致溶质质量分数变小,故需要密封保存.
答案:
(1)烧碱、火碱、苛性钠 2NaOH+H2SO4═Na2SO4+2H2O
(2)
①C
②2NaOH+CO2═Na2CO3+H2O
③浓盐酸具有挥发性
(1)氢氧化钠俗称为:烧碱、火碱、苛性钠等.氢氧化钠与硫酸反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O;
(2)
①滴加酚酞试液溶液变红,说明溶液显碱性,故含有氢氧化钠,碳酸钠虽然也显碱性,但由于加入了过量的氯化钙,所以溶液中无碳酸钠,故选C;
②氢氧化钠易与二氧化碳反应生成碳酸钠而变质,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
③浓盐酸具有挥发性,会导致溶质质量分数变小,故需要密封保存.
答案:
(1)烧碱、火碱、苛性钠 2NaOH+H2SO4═Na2SO4+2H2O
(2)
①C
②2NaOH+CO2═Na2CO3+H2O
③浓盐酸具有挥发性
点评:本题考查了常见物质的俗称及变质成分的探究和化学式和化学方程式的书写,完成此题,可以依据物质的性质进行.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
 如图是某广口瓶的标签,部分已经被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
如图是某广口瓶的标签,部分已经被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )| A、一定是Na2CO3 |
| B、一定是NaHCO3 |
| C、可能是Na2CO3,也可能是NaHCO3 |
| D、一定是Na2CO3和NaHCO3的混合物 |
如图是甲是初中化学炼铁的基本原理.乙是工业炼铁高炉的结构图.下列说法错误的是( )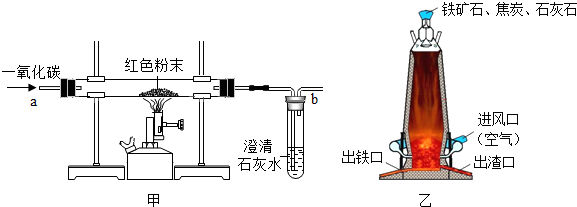

| A、由甲图加热装置可知炼铁需要高温 |
| B、乙图中焦炭燃烧产生高温也可以反应产生一氧化碳 |
| C、乙图中出铁口应该比出渣口高一些 |
| D、甲图中b处在操作时应该接尾气处理装置 |
在以下化学用语中,既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A、H |
| B、C60 |
| C、C |
| D、O2 |
可燃冰外观像冰,主要含甲烷水合物(由甲烷分子和水分子构成),还含有少量的二氧化碳气体.可燃冰属于( )
| A、化合物 | B、有机物 |
| C、混合物 | D、化石燃料 |
