题目内容
11.下面是钠元素和氯元素在元素周期表中的信息和三种粒子的结构示意图,试回答下列有关问题: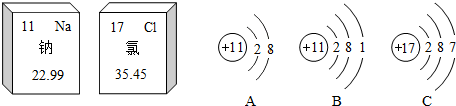
氯元素的核电荷数是17;A表示的粒子符号是Na+;B、C对应两种元素最本质的区别是质子数不同.
分析 根据元素周期表中所提供的氯元素信息结合原子序数=核电荷数分析氯元素的核电荷数;根据粒子结构示意图分析核内质子数和核外电子数的关系并结合离子符号的写分析;根据不同种元素最本质的区别是质子数不同分析.
解答 解:根据元素周期表中所提供的氯元素信息,可知氯元素的原子序数为17,又原子序数=核电荷数,因此氯元素的核电荷数是17;A微粒中质子数是11>核外电子数是10,因此该微粒是钠离子,符号是Na+;不同元素间最本质的区别是质子数不同,所以B和C表示的粒子最本质的区别是质子数不同.
故答案为:17;Na+;质子数不同.
点评 本题主要考查对元素周期表中信息的了解和应用,以及粒子结构示意图所表示出的信息和意义.

练习册系列答案
相关题目
1.下列指定反应的化学方程式正确的是( )
| A. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 铜和硝酸银反应:Cu+AgNO3═CuNO3+Ag↓ | |
| C. | 铜绿和稀盐酸反应:Cu2(OH)2CO3+4HCl═2CuCl2+3H2O+CO2↑ | |
| D. | 过氧化钠与二氧化碳反应生成纯碱和氧气:2Na2O2+CO2═2Na2CO3+O2↑ |
2.下列实验操作正确的是( )
| A. | 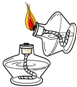 点燃酒精灯 | B. | 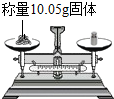 | C. | 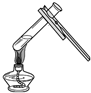 液体加热 | D. | 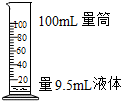 |
19.如图所示实验操作中正确的是( )
| A. | 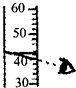 读出液体的体积 | B. | 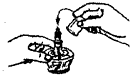 熄灭酒精灯 熄灭酒精灯 | C. | 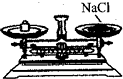 称量固体质量 | D. | 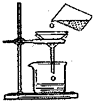 过滤 |
3.同学们用高锰酸钾制氧气.制取结束清洗仪器.发现加热高锰酸钾的试管内壁有用水洗刷不掉的黑色固体.
问题一:黑色固体是什么?
【交流讨论1】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
【实验验证1】向未洗净的试管中加入某种液体,产生能使带火星木条复燃的气体.证明上述判断正确.加入的液体是过氧化氢溶液.
问题二:用什么洗掉MnO2?
【交流讨论2】MnO2与Na2CO3、Ba(OH)2、Fe2O3、Zn中的某一种物质组成最相近,理由是二氧化锰和氧化铁都属于氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,由此推测MnO2也能与稀盐酸反应.
【实验验证2】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论3】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证3】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:产生了什么气体?
【交流讨论4】根据质量守恒定律,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证4】将该气体通入澄清石灰水中,发现澄清石灰水变浑浊,证明该气体是CO2.
问题一:黑色固体是什么?
【交流讨论1】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
| 判断 | 依据 |
| 不是KMnO4 | KMnO4能溶于水形成紫红色溶液 |
| 不是K2MnO4(填化学式) | 冲洗试管时出现深绿色溶液,说明该物质能溶于水 |
| 是MnO2 | 它是不溶于水的黑色固体 |
问题二:用什么洗掉MnO2?
【交流讨论2】MnO2与Na2CO3、Ba(OH)2、Fe2O3、Zn中的某一种物质组成最相近,理由是二氧化锰和氧化铁都属于氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,由此推测MnO2也能与稀盐酸反应.
【实验验证2】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论3】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证3】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:产生了什么气体?
【交流讨论4】根据质量守恒定律,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证4】将该气体通入澄清石灰水中,发现澄清石灰水变浑浊,证明该气体是CO2.
20.推理是一种重要的学习方法,下列推理正确的是( )
| A. | 化学变化都遵循质量守恒定律,所以质量不发生改变的变化就是化学变化 | |
| B. | 化合物是由多种元素组成的纯净物,所以由多种元素组成的纯净物一定是化合物 | |
| C. | 最外层达8电子的微粒化学性质稳定,因此化学性质稳定的微粒最外层电子数都是8 | |
| D. | 燃烧是发光、放热的变化,所以有发光、放热现象的变化一定是燃烧 |
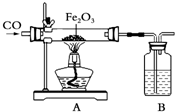 钢铁的冶炼是人类文明的一个重要标志,如图是模拟炼铁的实验装置图.
钢铁的冶炼是人类文明的一个重要标志,如图是模拟炼铁的实验装置图.