题目内容
2.除去下列各物质中少量杂质,所选用的试剂和操作方法均正确的是( )| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CaCO3(CaO) | 无 | 高温 |
| B | H2O(植物油) | 洗涤剂 | 振荡、搅拌 |
| C | CuO(铜粉) | 足量氧气 | 灼烧 |
| D | KCl(KClO3) | 二氧化锰 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CaCO3固体高温煅烧生成氧化钙和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、洗涤剂具有乳化作用,能将大的油滴分散成细小的油滴,振荡、搅拌后不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
C、铜粉在足量氧气中加热生成氧化铜,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、KClO3在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列过程中主要发生物理变化的是( )
| A. |  | B. | 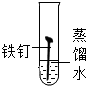 | C. | 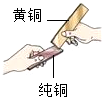 | D. | 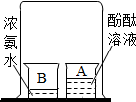 |
17.炒菜时加一点酒和醋能使菜味香可口,原因是有脂类物质生成.下列有关乙酸乙酯的叙述正确的是( )
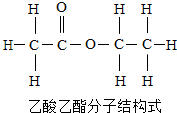

| A. | 乙酸乙酯是由碳、氢、氧元素组成的有机物 | |
| B. | 乙酸乙酯由碳、氢、氧原子构成 | |
| C. | 乙酸乙酯中碳、氧元素的质量比为2:1 | |
| D. | 乙酸乙酯中氧元素的质量分数最大 |
7.分类、类比是学习化学常用的方法.
(1)化学实验可按其主要目的分为:探究物质的性质、混合物的分离提纯,探究物质的含量等.因此应将下列实验中的B与C(填“A”或“C”或“D”)归为一类,依据是都属于混合物的分离.
(2)再反应C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO中,具有氧化性的反应物是二氧化碳.请写出一个两种化合物发生反应的化学方程式(其中一种化合物体现氧化性,另一种化合物体现还原性)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)化学实验可按其主要目的分为:探究物质的性质、混合物的分离提纯,探究物质的含量等.因此应将下列实验中的B与C(填“A”或“C”或“D”)归为一类,依据是都属于混合物的分离.
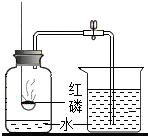 | 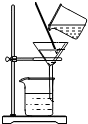 | 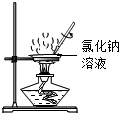 | 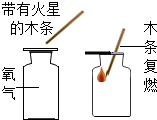 |
| A | B | C | D |
2.要除去下列物质中的少量杂质(括号内物质为杂质),下列实验方案设计中,不合理的是( )
| A. | CaCO3(CaCl2):加水溶解→过滤→洗涤→干燥 | |
| B. | N2(O2):将气体缓缓通过灼热的铜网 | |
| C. | NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 | |
| D. | KCl溶液(K2CO3):加入适量的稀盐酸 |
3. 水是生命之源,水与人类生活和生产密切相关.
水是生命之源,水与人类生活和生产密切相关.
(1)通过太阳能电池电解水获取氢能是绿色能源发展的方向.写出电解水的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
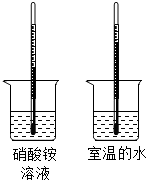
(2)物质溶于水,溶液的温度可能发生变化,观察图甲所示实验,判断硝酸铵溶于水时溶液的温度降低(填“升高”、“降低”或“不变”).
(3)水为最常见的溶剂.根据表中的数据,回答下列问题.
①20℃时,称取31.6g KNO3固体加入盛有100g水的烧杯中,充分溶解形成的溶液是饱和(填“饱和”或“不饱和”)溶液,称取31.6g KNO3固体时,发现托盘天平指针偏右,接下来的操作是继续加KNO3固体至天平平衡;
②当KNO3中混有少量NaCl时,提纯KNO3所采用的方法为降温结晶(或冷却热饱和溶液).
 水是生命之源,水与人类生活和生产密切相关.
水是生命之源,水与人类生活和生产密切相关.(1)通过太阳能电池电解水获取氢能是绿色能源发展的方向.写出电解水的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(2)物质溶于水,溶液的温度可能发生变化,观察图甲所示实验,判断硝酸铵溶于水时溶液的温度降低(填“升高”、“降低”或“不变”).
(3)水为最常见的溶剂.根据表中的数据,回答下列问题.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/ | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
②当KNO3中混有少量NaCl时,提纯KNO3所采用的方法为降温结晶(或冷却热饱和溶液).