题目内容
3.电解水时,常常要加入少量氢氧化钠增强导电性,使反应容易进行.现将240g4.5%氢氧化钠的水溶液进行电解,通电一段时间后,其中氢氧化钠的质量分数由4.5%变为5%.求电解水的质量(写出解题过程).分析 电解水的过程中氢氧化钠的质量不发生变化,所以可以根据氢氧化钠质量不变计算.
解答 解:设电解的水的质量为x.
240g×4.5%=(240g-x)×5%
x=24g
答:电解的水的质量为24g
点评 电解水的过程中加入的氢氧化钠或者硫酸,作用是提高导电能力,加速反应,过程中本身的质量不发生变化.

练习册系列答案
相关题目
13.元素周期表是学习和研究化学的重要工具,它的内容十分丰富.如图1所示是依据元素周期表画出的1~18号元素的原子结构示意图.我对它进行研究:
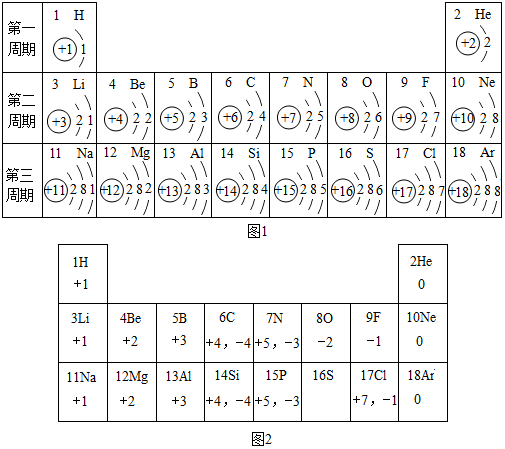
(1)原子序数为12的元素名称是镁,在化学反应中,该元素的原子容易失(填“得”或“失”)电子;原子序数为16的元素属于非金属(填“金属”或“非金属”)元素.
(2)我发现如下规律:
①原子序数与元素原子核电荷数在数值上相等;②同一纵行从上到下电子层数逐渐增加;③同一周期元素的原子的电子层数相同;
(3)此表纵行排列的依据是最外层电子数相同;此表横行排列的依据是电子层数相同;
(4)我猜想,第一纵行钠元素下的钾元素的原子结构示意图为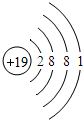 .
.
(5)进一步探究发现:原子结构与元素性质(特别是化学性质)关系非常密切,填写如表:

(1)原子序数为12的元素名称是镁,在化学反应中,该元素的原子容易失(填“得”或“失”)电子;原子序数为16的元素属于非金属(填“金属”或“非金属”)元素.
(2)我发现如下规律:
①原子序数与元素原子核电荷数在数值上相等;②同一纵行从上到下电子层数逐渐增加;③同一周期元素的原子的电子层数相同;
(3)此表纵行排列的依据是最外层电子数相同;此表横行排列的依据是电子层数相同;
(4)我猜想,第一纵行钠元素下的钾元素的原子结构示意图为
 .
.(5)进一步探究发现:原子结构与元素性质(特别是化学性质)关系非常密切,填写如表:
| 元素的分类 | 最外层电子数 | 得(或失)电子趋势 | 化学性质 |
| 稀有气体元素 | 8(氦为2) | 不易得失电子 | 比较稳定 |
| 金属元素 | 一般少于4 | 失电子 | 不稳定 |
| 非金属元素 | 一般多于或等于4个 | 得电子 | 不稳定 |
14.下列叙述正确的是( )
| A. | 由一种物质组成的物质是单质 | |
| B. | 在原子中,核内的质子数与核外的电子数不一定相等 | |
| C. | 原子里有相对很大的空间,电子在这个空间里作高速运动 | |
| D. | 在原子中,核内的质子数与中子数相等 |
11.下列微粒结构示意图中,表示阳离子的是( )
| A. | 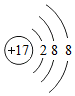 | B. | 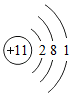 | C. | 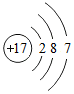 | D. | 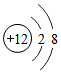 |
18.根据初中化学所学知识回答下列问题:
判断稀盐酸与下表中的四种化合物溶液之间能否发生反应.请仿照示例,在表格内②③④处填写(“能”或“不能”),并根据复分解反应发生的具体条件在对应的表格中填写判断依据.
判断稀盐酸与下表中的四种化合物溶液之间能否发生反应.请仿照示例,在表格内②③④处填写(“能”或“不能”),并根据复分解反应发生的具体条件在对应的表格中填写判断依据.
| 氢氧化钠溶液 | 氯化钠溶液 | 碳酸钾溶液 | 硝酸银溶液 | |
| 稀盐酸 | 示例:①能反应 | ②不能 反应 | ③能反应 | ④能 反应 |
| 判断依据 | 示例:有水生成 |
8.下列实验操作中,正确的是( )
| A. | 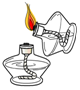 | B. | 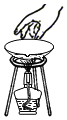 | C. | 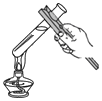 | D. | 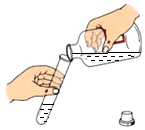 |
12.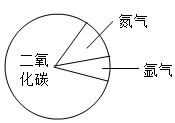 目前人类对火星的探测取得了重大的突破.如图是火星大气成分示意图,与空气的成分相比较,下列说法中正确的是( )
目前人类对火星的探测取得了重大的突破.如图是火星大气成分示意图,与空气的成分相比较,下列说法中正确的是( )
 目前人类对火星的探测取得了重大的突破.如图是火星大气成分示意图,与空气的成分相比较,下列说法中正确的是( )
目前人类对火星的探测取得了重大的突破.如图是火星大气成分示意图,与空气的成分相比较,下列说法中正确的是( )| A. | 火星大气中含有稀有气体而空气中没有 | |
| B. | 火星有了大气层也就同样适合人类生存 | |
| C. | 火星大气中氮气的体积分数大于空气中氮气的体积分数 | |
| D. | 火星大气中二氧化碳的体积分数大于空气中二氧化碳的体积分数 |
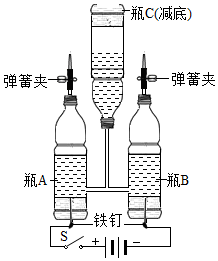 小周同学用塑料瓶、导管、铁钉、弹簧夹、胶水等制作了如图所示的简易电解水装置,进行家庭小实验.请根据要求回答下列问题:
小周同学用塑料瓶、导管、铁钉、弹簧夹、胶水等制作了如图所示的简易电解水装置,进行家庭小实验.请根据要求回答下列问题: