题目内容
14. 如图是二氧化碳的知识网络图(反应条件已略).
如图是二氧化碳的知识网络图(反应条件已略).(1)用化学符号填空:碳元素C;甲烷CH4;
碳酸中碳元素的化合价H2$\stackrel{+4}{C}$O3; 碳酸钙中所含阴离子CO32-;
(2)二氧化碳转化为碳酸钙的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
分析 (1)直接写出碳元素和甲烷的化学式,根据化合物中正负化合价的代数和为零来判断碳酸中碳元素的化合价,根据碳酸钠的构成来判断阴离子;
(2)根据二氧化碳与氢氧化钙反应生成碳酸钙和水,故可以据此答题.
解答 解:(1)碳元素的符号为:C,甲烷的化学式为CH4;
根据化合物中正负化合价的代数和为零,设碳酸中碳元素的化合价为x,则(+1)×2+x+(-2)×3=0,解得:x=+4.即碳酸中碳元素的化合价为+4,在标注化合价时将元素的化合价标在碳元素的正上方,故H2$\stackrel{+4}{C}$O3;
碳酸钠是由碳酸根和钠离子构成的化合物,所以其阴离子为碳酸根离子即:CO32-;
(2)二氧化碳与氢氧化钙反应生成碳酸钙和水,故可以写出该反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:
(1)C; CH4; ${H}_{2}{{\stackrel{+4}{C}}_{\;}}_{\;}$O3; CO32-;(2)CO2+Ca(OH)2═CaCO3↓+H2O.
点评 熟练掌握常见的元素符号、物质的化学式,能熟练的书写常见的化学方程式,书写时要标明反应条件、生成物的状态同时要注意配平.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列实验操作正确的是( )
| A. | 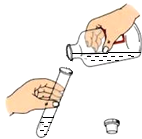 倾倒液体 | B. | 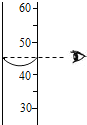 量取液体 | ||
| C. | 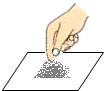 取粉末状固体 | D. | 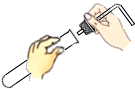 用橡皮塞塞住试管 |
5.金属的活动性顺序是一个重要的化学规律,这一规律的得出体现了实验和比较的方法在化学研究中的应用,下列比较不同金属活动性的实验方案合理的是( )
| A. | 取铝片和锌粉分别与质量分数相同的稀硫酸反应,反应速率大者活动性强 | |
| B. | 取表面积相等且经打磨的铝片和锌片分别与质量分数相同的稀硫酸反应,生成气体多者活动性强 | |
| C. | 取银粉和铜粉分别与质量分数相同的稀硫酸反应,反应速率大者活动性强 | |
| D. | 将铜丝伸入到硝酸银溶液中,如在铜丝表面附着一层灰黑色物质,说明铜的活动性大于银 |
2.某密闭容器中有X、02和NO三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表.根据表中信息,判断下列说法正确的是( )
| 物质 | X | O2 | NO | H20 |
| 反应前质量/g | 17 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 31 | 27 |
| A. | 该反应为置换反应 | B. | X的化学式可能是NH3 | ||
| C. | 表中“待测”值为36 | D. | 反应生成的NO和H20的个数比为3:2 |
19.下列有关溶液的说法中正确的是( )
| A. | 均一、稳定的液体都是溶液 | |
| B. | 饱和溶液一定比不饱和溶液浓 | |
| C. | 在其它条件不变时,氮气的溶解度随压强的升高而减小 | |
| D. | 餐具上的油污可利用洗涤剂的乳化功能将其洗去 |
3.下列变化属于化学变化的是( )
| A. | 轮胎爆炸 | B. | 电灯通电发亮 | C. | 葡萄酿成酒 | D. | 矿石粉碎 |
4.下列说法不利于改善本能地雾霾空气质量的是( )
| A. | 焚烧农作物秸秆、杂草 | B. | 多乘公交车,少来私家车 | ||
| C. | 工业废气处理达标后再排放 | D. | 大力治理公路、工地扬尘 |