题目内容
实验室废弃液中含一定量的AgNO3.兴趣小组同学回收金属银的流程如下: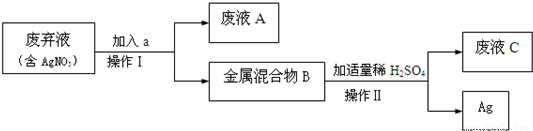
请认真分析以上流程,回答下列问题
(1)选择a.甲同学认为用铁,乙同学认为用铜,你认为 (选填“甲”或“乙”),你选择的理由是 ,加入a发生反应的化学方程式是 .
(2)讨论a的用量.经过讨论,同学们认为加入的a应该过量,加入过量a的目的是 ,请你写出证明加入的a过量的实验操作和现象 .
(3)金属混合物B与H2SO4反应的化学方程式为 .
【答案】分析:(1)由题意可知,甲同学得到的金属混合物含有银和铁,下一步易分离,所以科学;乙同学得到的金属混合物含有银和铜,不易分离,所以方案设计不合理;
(2)从铁的过量分析置换银的充分性,证明铁的过量即是证明B中含有金属铁,据此选择方法即可;
(3)根据金属混合物B的成分是铁和银,依据铁与稀硫酸反应的情况书写方程式即可;
解答:解:(1)由题意结合金属活动性顺序的应用可知,甲同学加入铁粉后得到的金属混合物含有银和铁,下一步加稀硫酸易分离,所以科学合理;乙同学得到的金属混合物含有银和铜,加稀硫酸两者均不能与之反应,所以不易分离,所以方案设计不合理;
(2)为能充分的置换出溶液中的银,可采用加入过量的铁粉进行实验,所以金属混合物B中含有的金属就是铁与银,证明铁的过量即是证明B中含有金属铁,可采用据此选择方法是取少量金属混合物B于试管中,滴入稀盐酸(或稀硫酸),有气泡产生即可;
(3)根据金属混合物B的成分是铁和银,依据铁与稀硫酸能反应但银与稀硫酸不能反应的情况;金属混合物B与H2SO4反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑
故答案为:(1)甲; 易与银分离(或铁在银中易被除去); Fe+2AgNO3═2Ag+Fe(NO3)2;
(2)使AgNO3中的银全部置换出来;取少量金属混合物B于试管中,滴入稀盐酸(或稀硫酸),有气泡产生;
(3)Fe+H2SO4=FeSO4+H2↑
点评:本题综合考查金属活动性顺序的应用、实验方案的设计与评价、化学方程式的书写等,解决的重点是金属活动性顺序的应用.
(2)从铁的过量分析置换银的充分性,证明铁的过量即是证明B中含有金属铁,据此选择方法即可;
(3)根据金属混合物B的成分是铁和银,依据铁与稀硫酸反应的情况书写方程式即可;
解答:解:(1)由题意结合金属活动性顺序的应用可知,甲同学加入铁粉后得到的金属混合物含有银和铁,下一步加稀硫酸易分离,所以科学合理;乙同学得到的金属混合物含有银和铜,加稀硫酸两者均不能与之反应,所以不易分离,所以方案设计不合理;
(2)为能充分的置换出溶液中的银,可采用加入过量的铁粉进行实验,所以金属混合物B中含有的金属就是铁与银,证明铁的过量即是证明B中含有金属铁,可采用据此选择方法是取少量金属混合物B于试管中,滴入稀盐酸(或稀硫酸),有气泡产生即可;
(3)根据金属混合物B的成分是铁和银,依据铁与稀硫酸能反应但银与稀硫酸不能反应的情况;金属混合物B与H2SO4反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑
故答案为:(1)甲; 易与银分离(或铁在银中易被除去); Fe+2AgNO3═2Ag+Fe(NO3)2;
(2)使AgNO3中的银全部置换出来;取少量金属混合物B于试管中,滴入稀盐酸(或稀硫酸),有气泡产生;
(3)Fe+H2SO4=FeSO4+H2↑
点评:本题综合考查金属活动性顺序的应用、实验方案的设计与评价、化学方程式的书写等,解决的重点是金属活动性顺序的应用.

练习册系列答案
相关题目
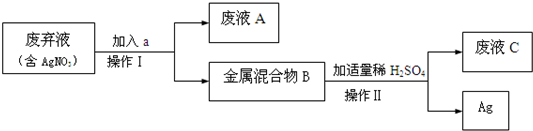

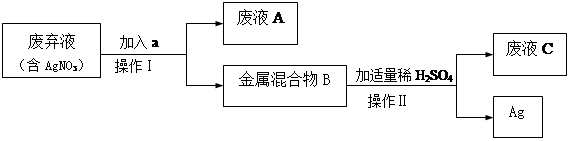
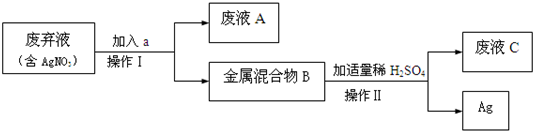
 程如下:
程如下: