题目内容
生活离不开水。某化学兴趣小组对学校附近河流水质的状况进行调查研究。
(1)要除去水样中的不溶物,可采取的操作是______。
(2)完成(1)中的操作后,可用________检验所得水样属于硬水还是软水。
(3)完成(2)中的操作后,测定水样为硬水。日常生活中,当水的硬度大并且担心病菌过多时,可以采取______的方法降低水的硬度和杀灭病菌。
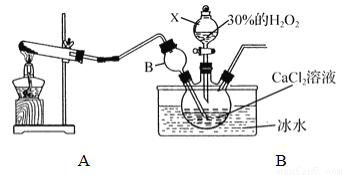
(4)ClO2是一种安全的饮用水消毒剂,生产ClO2的化学反应方程式为 2NaClO2 + X== 2ClO2 + 2NaCl ,方程式中X的化学式为________。
(5)爱护水资源是公民的责任和义务。下列行为不属于节约用水的是_______。
A.用未经处理的工业废水浇地 B.洗衣机洗衣服时不间断地边注水边冲洗、排水
C.洗过菜的水用来浇花 D.农业和园林浇灌改大水浸灌为喷灌、滴灌
过滤 肥皂水 加热 Cl2 C 、D 【解析】(1)要除去水样中的不溶物,可采取的操作是过滤;(2)检验所得水样属于硬水还是软水,可用的物质是肥皂水,遇肥皂水产生的泡沫少的是硬水,遇肥皂水产生的泡沫多的是软水;(3)在日常生活中将硬水转化为软水的方法是煮沸;(4)根据X+2NaClO2=2ClO2+2NaCl可知生成物中有2个钠原子、4个氯原子、4个氧原子、在反应物中有2个钠原子、4个氧原子...
练习册系列答案
相关题目



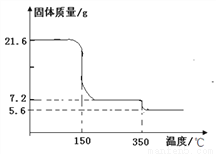
 CaO2·yH2O↓+NH4Cl。
CaO2·yH2O↓+NH4Cl。