题目内容
3. 在实验室中,化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸成分反应,测得部分数据与图象如下,请根据有关信息回答问题.
在实验室中,化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸成分反应,测得部分数据与图象如下,请根据有关信息回答问题.| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
| 锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(2)b的数值为2.2;
(3)计算该试剂中氢氧化钙的质量分数.(写出计算过程,结果保留一位小数.)
分析 (1)根据表中的数据的变化特点分析a的值;
(2)由表中的数据可知,第6次加入盐酸的质量就等于锥形瓶增加的质量,说明了第5次加入的盐酸已将碳酸钙完全反应,则生成的二氧化碳的质量:150g+25g-172.8g=2.2g;
(3)根据碳酸钙与盐酸的反应,由二氧化碳的求出碳酸钙的质量,即可求出氢氧化钙的质量分数.
解答 解:(1)由表中的数据可知,第1、2、4次加入盐酸的质量就等于锥形瓶中增加的质量,所以第3次加入盐酸后物质的质量就是2次锥形瓶中物质的质量再加上盐酸的质量,故a的值为:100g+25g=125g.
(2)由表中的数据可知,第6次加入盐酸的质量就等于锥形瓶增加的质量,说明了第5次加入的盐酸已将碳酸钙完全反应,则生成的二氧化碳的质量:150g+25g-172.8g=2.2g
(3)设需要碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
解得:x=5g
试剂中氢氧化钙的质量分数为:$\frac{19.8g-5g}{19.8g}$×100%≈74.7%
故答案为:(1)125;
(2)2.2;
(3)氢氧化钙的质量分数为74.7%.
点评 根据数据列表或关系图,找出反应中某物质的质量是这一类问题的解决方法.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
13.下列收集O2的方法错误的是( )
| A. | 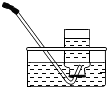 | B. | 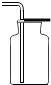 | C. | 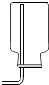 | D. | 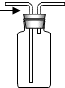 |
14.下列有关化学知识的叙述Ⅰ和叙述Ⅱ均正确并有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | KNO3的溶解度大 | 用蒸发结晶法除去KNO3中混有少量的NaCl |
| B | AgCl难溶于水 | 用稀硝酸和Ag NO3溶液检验Cl- |
| C | 在食物中可适量使用食品添加剂 | 食品添加剂都是用来增加食物的营养成分的 |
| D | Ca(OH)2能制成澄清石灰水 | 可配制溶质质量分数为20%的Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
11.小明同学在家里用洁厕液清洁陶瓷卫生洁具,发现洁具上的水垢快速消失,并有气泡产生.他联系化学课上所学知识,与同学们在实验室围绕“洁厕液”探究了以下问题.
评价与反思:小花同学对上述问题二设计了不同的方案,得出了洁厕液与炉具清洁剂之间能发生化学反应,二者不能混合使用的结论.她设计的方案是取适量炉具清洁剂于试管中,滴加几滴酚酞试液,酚酞试液变红色,再滴加洁厕液,边滴加边振荡,红色褪去.(写出操作方法及实验现象)
拓展探究:请你围绕“洁厕液”再提出一个值得探究的问题洁厕液能够清洗大理石地板吗.
总结延伸:除了以上探究的问题,你认为在使用洁厕液时还应该注意不要溅到皮肤上.(写出一条即可)
| 提出问题 | 作出猜想 | 实验验证 | 实验现象 | 得出结论 |
| 问题一:洁厕液是酸性还是碱性? 查阅资料:水垢的主要成分为碳酸钙和氢氧化镁. | 洁厕液显酸性,他作出此猜想的依据是 碳酸钙能和显酸性的物质反应生成二氧化碳气体,氢氧化镁能和显酸性的物质反应. | 用pH试纸检测其酸碱度,方法是 用洁净干燥的玻璃棒蘸取处理后的废水,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH | pH=2 | 洁厕液显酸性.(老师提示:主要成分为盐酸)通过实验可知:用pH试纸检测溶液的酸碱度时,应注意pH试纸要保持干燥 用洁厕液除水垢时,产生气泡的化学反应方程式是 CaCO3+2HCl═CaCl2+H2O+CO2↑ |
| 将洁厕液加水稀释后,再次检测pH. | 测得pH 大于2(填“大于”“小于”或“等于”) | |||
| 问题二:洁厕液能与炉具清洁剂混合使用吗? 查阅资料:炉具清洁剂主要成分为氢氧化钠 | 二者能混合使用,并能提高清洁效果. | 将洁厕液倾倒入一支试管中,向其中滴加炉具清洁剂 | 没有观察到任何现象 | 二者之间不发生化学反应.混合使用能同时除去水垢和油污. |
拓展探究:请你围绕“洁厕液”再提出一个值得探究的问题洁厕液能够清洗大理石地板吗.
总结延伸:除了以上探究的问题,你认为在使用洁厕液时还应该注意不要溅到皮肤上.(写出一条即可)
8.如图是某反应的微观示意图,分析错误的是( )


| A. | 该反应属于化合反应 | B. | 每个生成物分子由3个原子构成 | ||
| C. | 该反应中反应物的质量比为1:2 | D. | 两种反应物均为单质 |
15. 一定量的碳与氧化铜混合加热,反应前后测定装置I、Ⅱ的质量如下.分析错误的是( )
一定量的碳与氧化铜混合加热,反应前后测定装置I、Ⅱ的质量如下.分析错误的是( )
 一定量的碳与氧化铜混合加热,反应前后测定装置I、Ⅱ的质量如下.分析错误的是( )
一定量的碳与氧化铜混合加热,反应前后测定装置I、Ⅱ的质量如下.分析错误的是( )| 反应前质量(g) | 反应后质量(g) | |
| 装置I | 56.3 | 55.2 |
| 装置II | 242.9 | 243.7 |
| A. | 生成的气体是混合物 | |
| B. | I中减少的质量是氧元素的质量 | |
| C. | 反应后I中固体成分可能有3种情况 | |
| D. | Ⅱ中增加的质量是吸收的二氧化碳的质量 |
15.下列物质的用途主要利用其物理性质的是( )
| A. | 氧气用于医疗急救 | B. | 氢气作清洁燃料 | ||
| C. | 熟石灰用于改良酸性土壤 | D. | 石墨作电池电极 |