题目内容
18.某化学实验小组实验结束时,将含有CuSO4、ZnSO4、FeSO4的废液倒入废液缸中,为回收有关金属和盐,同学们设计了如下实验方案:
(1)固体B为铁,固体D为铜.
(2)步骤①中的两反应的化学方程式为Zn+CuSO4═ZnSO4+Cu,Zn+FeSO4═ZnSO4+Fe.
分析 根据图框可知:锌与CuSO4反应生成ZnSO4和铜;锌与FeSO4反应生成ZnSO4和铁;故滤液A为硫酸锌溶液;固体A中铁被磁铁吸出,故固体B为铁,而固体C为铜、锌,故可推测固体D为铜,滤液B为硫酸锌;则可根据反应物、生成物及其质量守恒定律可以书写化学方程式.
解答 解:根据图框可知:锌与CuSO4反应生成ZnSO4和铜;锌与FeSO4反应生成ZnSO4和铁;故滤液A为硫酸锌溶液;固体A中铁被磁铁吸出,故固体B为铁,而固体C为铜、锌,故可推测固体D为铜,滤液B为硫酸锌.
(1)固体B为铁,固体D为铜.
(2)锌和硫酸铜反应能生成硫酸锌和铜,锌和硫酸亚铁反应能生成硫酸锌和铁,反应的化学方程式分别为:Zn+CuSO4═ZnSO4+Cu、Zn+FeSO4═ZnSO4+Fe;
故答案为:
(1)铁,铜;
(2)Zn+CuSO4═ZnSO4+Cu;Zn+FeSO4═ZnSO4+Fe;
点评 掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力;熟记常用化学方程式.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
9.下列变化中与其它不同的是( )
| A. | 消化食物 | B. | 焚烧垃圾 | C. | 冰块融化 | D. | 食盐水制氯气 |
3.通过化学课的学习,成语“细水长流”可理解为( )
| A. | 在家刷牙洗脸时,让水细细的不间断的留着 | |
| B. | 水管漏水时让其“细水长流”,方便使用 | |
| C. | 节约每一滴水,形成“细水长流”的水资源观 | |
| D. | 地球淡水资源丰富,可供长久使用 |
7.实验室常用的下列仪器中,属于复合材料的是( )
| A. |  集气瓶 | B. |  坩埚钳 | C. |  石棉网 | D. |  试管架 |
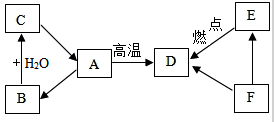 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易于血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:
已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易于血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答: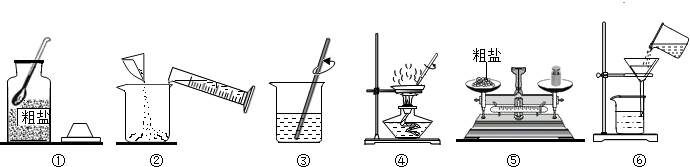
 将下列各仪器名称前的字母按其用途填在相应位置.(1)贮存固体药品的仪器是B;
将下列各仪器名称前的字母按其用途填在相应位置.(1)贮存固体药品的仪器是B;