题目内容
5.下列叙述不正确的是( )| A. | 铜、铁、银相比导电性最好的是银 | |
| B. | 铁和铝都能跟稀硫酸发生置换反应,铜不可以 | |
| C. | 铁制品非常坚固,不易损坏,不能变质 | |
| D. | 铁器能被磁铁吸引 |
分析 A、可以根据金属的性质方面进行分析、判断,从而得出正确的结论.
B、依据金属与酸反应的规律情况分析解答,主要是利用金属活动性在氢前的金属可以与稀酸发生置换反应的知识解决.
C、考虑铁制品容易生锈;
D、磁化材料是容易被磁化的物质,如铁、钴、镍.生活中具有这些磁性材料的物体,都容易被磁铁吸引.
解答 解:A、铜、铁、银相比导电性最好的是银.故正确;
B、根据金属活动性顺序可知,铁和铝都能跟稀硫酸发生置换反应,铜不可以.故正确;
C、铁制品容易生锈,容易损坏变质.故错误;
D、铁器能被磁铁吸引.故正确.
故选C.
点评 解答本题的关键是要充分理解金属的物理性质,只有这样才能对金属的性质和用途等方面的问题做出正确的判断.

练习册系列答案
相关题目
15.某化学活动小组用如图所示实验装置探究氨气(NH3)的性质、测定氧化铜试样中氧化铜的质量分数(其中杂质不发生变化,装置中的每一步处理都是完全的),充分反应后观察到C装置中的固体由黑色转变为亮红色.
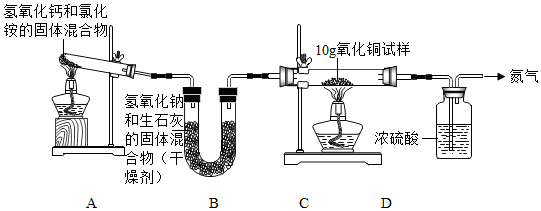
试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
10g氧化铜样品中氧化铜的质量是8g;
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.

试回答下列问题:
(1)氮气的密度和空气相似,难溶解于水,实验室收集氮气的方法是A
A.排水集气法 B.向上排空气集气法 C.向下排空气集气法
(2)A装置中的试管口要略低于试管底部的原因是防止冷凝水倒流炸裂试管;
(3)反应前后C、D装置的质量为:
| C装置总质量 | D装置总质量 | |
| 实验前 | 160g | 200g |
| 实验后 | 158.4g | 201.8g |
(4)写出C装置的玻璃管内发生反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
1.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈性,还可能呈性.
【实验验证】
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入CuCl2溶液,直到不再产生沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为CuCl2+2NaOH═Cu(OH)2↓+2NaCl.
(2)若无色酚酞试液不变色,此时试管中的溶质(除酚酞外)可能有两种情况:
①溶质是NaCl(填化学式,下同);
②溶质是HCl、NaCl.
③若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为Zn+2HCl═ZnCl2+H2↑;若无明显现象,则呈中性.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈性,还可能呈性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入CuCl2溶液,直到不再产生沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为CuCl2+2NaOH═Cu(OH)2↓+2NaCl.
(2)若无色酚酞试液不变色,此时试管中的溶质(除酚酞外)可能有两种情况:
①溶质是NaCl(填化学式,下同);
②溶质是HCl、NaCl.
③若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为Zn+2HCl═ZnCl2+H2↑;若无明显现象,则呈中性.
2.一种焰火火药中所含的硝酸铜在燃放时产生绿色火焰,发生如下反应:2Cu(NO3)2═2CuO+O2↑+4X↑.下列有关说法错误的是( )
| A. | X的化学式为NO2 | |
| B. | 该反应的基本反应类型为分解反应 | |
| C. | 该反应前后元素的化合价没有发生改变 | |
| D. | 产物中CuO属于氧化物 |

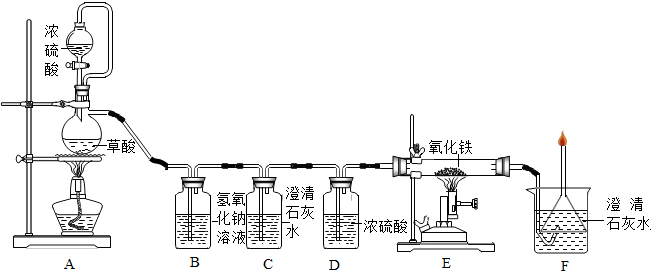 其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是H2C2O4$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$H2O+CO2↑+CO↑.
其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是H2C2O4$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$H2O+CO2↑+CO↑.