题目内容
图为“XX”钙片商品标签图,请根据标签的有关信息完成下列各题.
(1)每片钙片中至少含钙元素的质量为______g.
(2)小花同学为测定其中碳酸钙的含量标注是否属实,她取出10片钙
片,研碎后放入小烧杯中,再加入50g足量稀盐酸,在T。至T3时间段,
测得反应剩余物的质量变化如下:
| 时间 | T0 | T1 | T2 | T3 |
| 反应剩余物质量(g) | 70 | 65 | 63.4 | 63.4 |
① 生成的二氧化碳的质量是多少?②通过计算判断该钙片中碳酸钙的含量标注是否属实.
解:(1)1.5g×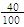 ×100%=0.6g 2分
×100%=0.6g 2分
(2)①10片×2g/片+50g-63.4g=6.6g 1分
②设含碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 6.6g

X=15g 2分
每片中含有碳酸钙的质量为: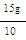 =1.5g,符合要求.
=1.5g,符合要求.
答:(1)生成二氧化碳质量为6.6g
(2)钙片含碳酸钙的含量标注属实. 1分

医务人员用3%的过过氧化氢溶液为伤者处理伤口时,伤口上会看到大量的气泡.下列有关说法中正确的是( )
|
| A. | 生成的气体一定是过氧化氢分解产生的氢气 |
|
| B. | 伤口处的生物酶可能对氧化氢的分解起到催化作用 |
|
| C. | 只有二氧化锰能使过氧化氢在常温下迅速分解 |
|
| D. | 过氧化氢和水的分子构成不同,所以他们的性质完全不同 |
在电解水的实验中可以直接观察到的现象是( )
|
| A. | 有氢气和氧气产生,且体积比为2:1 |
|
| B. | 水是由氢氧两种元素组成 |
|
| C. | 两电极均冒气泡,负极管内气体和正极管内气体的体积之比约为2:1 |
|
| D. | 每个水分子是由两个氢原子和一个氧原子构成的 |
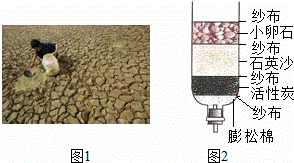
 。
。 内壁水垢[主要含CaCO3和Mg(OH)2]的是 ;
内壁水垢[主要含CaCO3和Mg(OH)2]的是 ;