题目内容
5.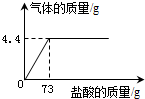 向13.6g碳酸钠和氯化钠的固体混合物滴加稀盐酸,所加稀盐酸质量与生成气体质量的关系如图所示.计算:
向13.6g碳酸钠和氯化钠的固体混合物滴加稀盐酸,所加稀盐酸质量与生成气体质量的关系如图所示.计算:(1)生成的二氧化碳的质量为4.4g.
(2)该稀盐酸中溶质的质量分数.(计算结果精确至0.1%)
分析 根据题给的条件可以知道所发生的反应为碳酸钠和盐酸的反应,而生成二氧化碳气体的质量为4.4g,可以据此来分析求算参加反应的盐酸的质量.
解答 解:(1)由图示可知,生成二氧化碳气体的质量为4.4g;
设参加反应稀盐酸中溶质的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
y 4.4g
$\frac{73}{y}$=$\frac{44}{4.4g}$
y=7.3g
稀盐酸中溶质的质量分数为:$\frac{7.3g}{73g}$×100%=10.0%.
故答案为:(1)4.4g;
(2)10.0%.
点评 本题通过计算的形式考查了碳酸盐与盐酸的反应,难度不大,关键是正确理解反应的原理.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案
相关题目
10.下列关于燃烧现象的描述中正确的是( )
| A. | 木炭在空气中燃烧后,生成黑色的固体 | |
| B. | 铁丝在氧气中燃烧发出明亮的火焰 | |
| C. | 镁条在空气中燃烧,发出耀眼的白光 | |
| D. | 红磷在空气中燃烧,产生蓝紫色火焰 |
15.下列实验数据正确的是( )
| A. | 天平称物质质量为 12.52g | B. | 天平称物质质量为 12.0g | ||
| C. | 量筒量得液体体积为12.35mL | D. | 量筒量得液体体积为12.30mL |
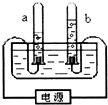 如图是实验室电解水的装置,请看图回答下列问题:
如图是实验室电解水的装置,请看图回答下列问题: