题目内容
5.现有盐酸、氢氧化钠、氢氧化钙三瓶遗失标签的溶液,为了鉴别这些溶液,将它们随机编号为A、B、C,并按图步骤进行实验,观察到以下现象: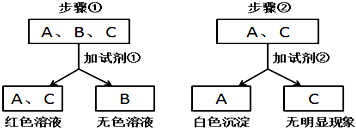
(1)试剂①的名称是酚酞试液;溶液B中溶质的化学式是HCl.
(2)若试剂②是气体,则试剂②的化学式为CO2,生成白色沉淀的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(3)写出A与B反应的化学方程式:Ca(OH)2+2HCl=CaCl2+2H2O.
分析 根据氢氧化钠和氢氧化钙都是碱,都显碱性,会使酚酞变红色,盐酸显酸性不会使酚酞变红色,氢氧化钠和氢氧化钙中阳离子不同,可以加入二氧化碳、碳酸钠等,在氢氧化钙中会生成白色沉淀,在氢氧化钠中没有现象,根据推出的反应物、生成物书写方程式;据此完成相关的问题.
解答 解:(1)氢氧化钠和氢氧化钙都是碱,都显碱性,会使酚酞变红色,盐酸显酸性不会使酚酞变色,因此试剂①是酚酞试液,A和C分别是氢氧化钠、氢氧化钙中的一种,而B是盐酸;
故答案为:酚酞试液;HCl;
(2)氢氧化钠和氢氧化钙中阳离子不同,若试剂②是气体,二氧化碳能够和氢氧化钙反应产生沉淀,和氢氧化钠反应无现象,因此试剂②是二氧化碳,反应的方程式为:;
故答案是:CO2;Ca(OH)2+CO2=CaCO3↓+H2O;
(3)由现象可知,A是氢氧化钙,B是盐酸,C是氢氧化钠;
A和B反应是氢氧化钙和盐酸反应生成氯化钙和水,其反应化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
故答案是:Ca(OH)2+2HCl=CaCl2+2H2O.
点评 本题考查了酸碱的鉴别,在解此类题时,首先分析需要鉴别的物质的性质,然后选择适当的试剂,出现不同的现象即可鉴别.

练习册系列答案
相关题目
16.生活中处处有化学,下列说法错误的是( )
| A. | 医疗上常用体积分数为70%的酒精作消毒剂 | |
| B. | 长期过量摄入食盐,会引起高血压等病症 | |
| C. | 汽车安装尾气净化装置,以节约石油资源 | |
| D. | 经常使用染发剂,不利于身体健康 |
20.下列各组物质的两种鉴别方法,都正确的是( )
| 序号 | 物质 | 方法一 | 方法二 |
| A | 一氧化碳和二氧化碳 | 闻气味 | 通过石灰水 |
| B | 硝酸铵和磷矿粉 | 看颜色 | 加入足量水 |
| C | 稀盐酸和稀硫酸 | 滴加氯化钡溶液 | 滴加紫色石蕊溶液 |
| D | 铜粉和氧化铁粉末 | 用磁铁吸引 | 加稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |

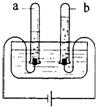 如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b. 请回答:
如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b. 请回答: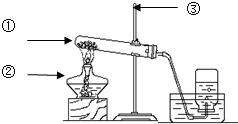 如图是用高锰酸钾制取氧气的实验装置图,请回答:
如图是用高锰酸钾制取氧气的实验装置图,请回答: