题目内容
20.饮用天然水时,为了防止水中的微生物造成疾病传播,需将天然水处理之后方可饮用.常用的处理措施有:①加热煮沸②过滤③杀菌④自然沉降,合理的处理顺序是( )| A. | ③①②④ | B. | ④①②③ | C. | ④②③① | D. | ③①④② |
分析 可以根据净化水的方法方面进行分析、判断,从而得出正确的结论.
解答 解:自然沉降能除去水中含有的大颗粒不溶性固体,过滤能除去不溶性小颗粒固体,消毒能除去水中的细菌微生物,加热煮沸能减少水中的可溶性固体.
故选C.
点评 解答本题的关键是要充分理解净化水的方法,只有这样才能对问题做出正确的判断.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
11.BaCl2是一种有毒的盐,误食了BaCl2可用下列哪种物质作解毒剂( )
| A. | AgCl | B. | MgSO4 | C. | Na2SO4 | D. | BaCO3 |
8.有一包白色粉末,可能由硝酸铜、硫酸钠、碳酸钠、氯化钡、氢氧化钠中的一种或几种组成.某化学兴趣小组的同学们为探究其组成,设计并进行了以下实验:
请分析实验过程,回答下列问题:
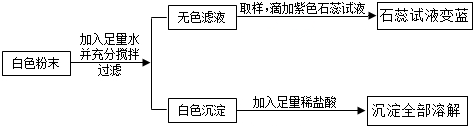
(1)白色粉末中一定不含CuSO4、Na2SO4(填写化学式).
(2)请你写出生成白色沉淀的化学方程式为BaCl2+Na2CO3=2NaCl+BaCO3↓.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】
猜想Ⅰ:碳酸钠
猜想Ⅱ:氢氧化钠
猜想Ⅲ:碳酸钠和氢氧化钠
【设计实验】
【收集证据】
①若现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅱ不成立.
②若现象A是有白色沉淀生成,X溶液为氯化钡;取反应后的上层清夜,测定其pH,当pH>7(选填“>”或“<”或“=”),则猜想Ⅲ成立.
【进行实验】兴趣小组的同学们依据设计的实验进行探究,得出白色粉末的组成.
【实验反思】实验中需滴加足量X溶液的目的是为了使得反应充分,避免对后续试验造成影响.
请分析实验过程,回答下列问题:

(1)白色粉末中一定不含CuSO4、Na2SO4(填写化学式).
(2)请你写出生成白色沉淀的化学方程式为BaCl2+Na2CO3=2NaCl+BaCO3↓.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】
猜想Ⅰ:碳酸钠
猜想Ⅱ:氢氧化钠
猜想Ⅲ:碳酸钠和氢氧化钠
【设计实验】
| 实验操作 | 实验现象 |
| 取无色滤液少许于试管中,滴加足量的X溶液 | 观察到现象A |
①若现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅱ不成立.
②若现象A是有白色沉淀生成,X溶液为氯化钡;取反应后的上层清夜,测定其pH,当pH>7(选填“>”或“<”或“=”),则猜想Ⅲ成立.
【进行实验】兴趣小组的同学们依据设计的实验进行探究,得出白色粉末的组成.
【实验反思】实验中需滴加足量X溶液的目的是为了使得反应充分,避免对后续试验造成影响.
5.举重前,运动员会用碳酸镁白色粉末摩擦掌心,增大掌心与器械的摩擦.碳酸镁属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
10.下列有关实验现象的描述正确的是( )
| A. | 红磷在氧气中燃烧产生大量的白烟 | |
| B. | 铁丝在空气中剧烈燃烧时,火星四射,生成黑色固体 | |
| C. | 打开盛有浓硫酸的试剂瓶的瓶盖,瓶口上方出现大量白雾 | |
| D. | 将碘酒滴入淀粉溶液中,溶液变紫色 |