题目内容
4.有三瓶无色无味的气体,分别是氧气,空气,二氧化碳,区别他们最简单的方法是( )| A. | 测定气体的密度 | B. | 滴入澄清石灰水,震荡 | ||
| C. | 深入燃烧的木条 | D. | 滴入紫色石蕊试液,震荡 |
分析 区别空气、氧气和二氧化碳三瓶无色气体,要求根据三种气体性质差别,所设计的方案能出现三种明显不同的实验现象,达到鉴别气体的目的.
解答 解:A、三种气体密度不同,测三瓶气体的密度可以区别三种气体,但不是最简单方法;故A错误,
B、倒入澄清石灰水,石灰水变浑浊的气体为二氧化碳,无明显现象的为空气或氧气.无法区别三种气体,故B错误,
C、燃着的木条分别放入瓶中,燃烧无明显变化的气体为空气;燃烧更旺的气体为氧气;燃烧熄灭的气体为二氧化碳;故C正确,
D、倒入紫色石蕊试液,使溶液变红的气体为二氧化碳,无明显现象的为空气或氧气.无法区别三种气体,故D错误,
故选C.
点评 利用所要鉴别物质的性质差别,设计实验,实验中出现明显的现象差异,达到鉴别物质的目的.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
16.地球上的金属资源广泛地存在于地壳和海洋中,工业上主要是从含有金属元素并有开采价值的矿石中提炼金属.
(1)赤铁矿在自然界中储藏丰富,其主要成分的化学式是Fe2O3.
(2)工业上主要采用高炉炼铁,常用到的原料有铁矿石、焦炭、石灰石和空气.其中,焦炭的作用是燃烧提供热量(产生一氧化碳).(仅答一点)
(3)由于铁的氧化物中Fe3O4和FeO均为黑色,实验室用CO还原Fe2O3得到的铁中是否会含有Fe3O4和FeO,某同学设计了下列探究实验.
资料:FeCl3溶液与铁发生的反应是2FeCl3+Fe═3FeCl2,但FeCl3溶液不与Fe3O4、FeO反应;含有Fe3+的盐溶液遇到KSCN溶液时变成红色,利用该反应可检验Fe3+的存在.
【提出问题】CO还原Fe2O3得到黑色产物的成分是什么?
【猜想】
猜想l:Fe 猜想2:Fe和Fe3O4;
猜想3:Fe和FeO; 猜想4:Fe、FeO、Fe3O4
【实验探究】限选试剂:C0、盐酸、澄清石灰水、KSCN溶液、FeCl3溶液.
(1)赤铁矿在自然界中储藏丰富,其主要成分的化学式是Fe2O3.
(2)工业上主要采用高炉炼铁,常用到的原料有铁矿石、焦炭、石灰石和空气.其中,焦炭的作用是燃烧提供热量(产生一氧化碳).(仅答一点)
(3)由于铁的氧化物中Fe3O4和FeO均为黑色,实验室用CO还原Fe2O3得到的铁中是否会含有Fe3O4和FeO,某同学设计了下列探究实验.
资料:FeCl3溶液与铁发生的反应是2FeCl3+Fe═3FeCl2,但FeCl3溶液不与Fe3O4、FeO反应;含有Fe3+的盐溶液遇到KSCN溶液时变成红色,利用该反应可检验Fe3+的存在.
【提出问题】CO还原Fe2O3得到黑色产物的成分是什么?
【猜想】
猜想l:Fe 猜想2:Fe和Fe3O4;
猜想3:Fe和FeO; 猜想4:Fe、FeO、Fe3O4
【实验探究】限选试剂:C0、盐酸、澄清石灰水、KSCN溶液、FeCl3溶液.
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ取少量黑色产物加入到装有足量FeCl3溶液的烧杯中,充分反应后过滤,对过滤所得固体用蒸馏水洗涤. | 黑色固体部分溶解. | 猜想2和4都 不成立. |
| Ⅱ取少量操作Ⅰ所得的滤渣于试管中,再加入足量的稀盐酸,充分反应后,再加入适量的KSCN溶液. | 黑色固体全部溶解,溶液 不变红色. | |
| Ⅲ另取少量黑色产物装入玻璃管中,通入C0,一段时间后加热,并将反应后的气体通入装有一定量的澄清石灰水 的烧杯中. | 澄清石灰水变浑浊. | 猜想l不成立, 猜想3成立. |
13.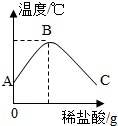 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )| A. | 稀盐酸与氢氧化钠溶液发生的中和反应是放热反应 | |
| B. | 从A到B过程中,烧杯中溶液的pH逐渐减小 | |
| C. | B点时,往烧杯中滴加无色酚酞试液,溶液变红色 | |
| D. | C点时烧杯中含有的溶质是NaCl,HCl |

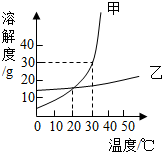 如图是甲、乙两种固体物质的溶解度曲线从图中你能获得的信息有:
如图是甲、乙两种固体物质的溶解度曲线从图中你能获得的信息有: