题目内容
4.向一定质量的K2CO3、K2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示.下列说法正确的是( )
| A. | 取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量 | |
| B. | c点沉淀的成分为一种 | |
| C. | o~a段发生了一个反应 | |
| D. | m=2.33 |
分析 根据碳酸钠与氯化钡反应会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡反应生成不溶于酸得硫酸钡沉淀,依据图象这沉淀的质量和二氧化碳气体的质量进行计算分析.
解答 解:碳酸钠与氯化钡反应会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡反应生成不溶于酸得硫酸钡沉淀,所以
A、取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,加入的氯化钡会引入氯离子所以不能说明盐酸过量,故选项错误;
B、c点时,沉淀质量不再减少,说明碳酸钡被反应完,所以此时沉淀是硫酸钡沉淀,故选项正确;
C、o-a段发生的反应是碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠两个反应,故选项错误;
D、设参加反应的碳酸钡沉淀质量为x
BaCO3---CO2,
197 44
x 0.88g
$\frac{197}{x}$=$\frac{44}{0.88g}$
x=3.94g
所以m=6.27g-3.94g=2.33g,故选项正确;
故选:BD.
点评 本题属于实验探究题,综合性较强,既有试验探究,又有实验数据图象的分析.只有综合掌握了基础知识才能较好的完成本类练习题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.在一定温度下,食盐的饱和溶液一定是( )
| A. | 很浓的溶液 | B. | 不能继续溶解氯化钠的溶液 | ||
| C. | 很稀的溶液 | D. | 不能继续溶解其他物质的溶液 |
15.若用“ ”表示氮原子,下列方框中,符合2N2的示意图是( )
”表示氮原子,下列方框中,符合2N2的示意图是( )
 ”表示氮原子,下列方框中,符合2N2的示意图是( )
”表示氮原子,下列方框中,符合2N2的示意图是( )| A. | 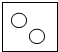 | B. |  | C. | 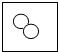 | D. | 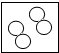 |
12.下列物质可使无色酚酞试液变红的是( )
| A. | 食盐水 | B. | 稀硫酸 | C. | 碳酸钠溶液 | D. | 盐酸 |
16.在化学符号:①NO2 ②2CO ③Ca2+ ④H2O2 ⑤2OH- ⑥$\stackrel{+2}{Zn}$SO4中,关于数字“2”的意义,下列说法错误的是( )
| A. | 表示分子个数的是② | |
| B. | 表示离子所带电荷数的是②⑤ | |
| C. | 表示化合价数值的是⑥ | |
| D. | 表示一个分子中所含某种原子个数的是①④ |
13.下列鉴别物质所用的试剂或方法,错误的是( )
| A. | 氧气和氮气-燃着的木条 | B. | 氯化钠和硝酸铵-用水 | ||
| C. | 锌片和银片-硫酸铜溶液 | D. | 碳酸钠粉末和碳酸钙粉末-稀盐酸 |
1.下列物质属于纯净物的是( )
| A. | 洁净的空气 | B. | 精制的食盐水 | C. | 冰水混合物 | D. | 澄清石灰水 |