题目内容
有一种石灰石样品(主要成分为CaCO3).其中含有二氧化硅杂质(二氧化硅不溶于水,不与盐酸反应).某学生取2g这种石灰石样品,把25g盐酸分5次加入,充分反应后剩余固体的质量见下表(发生反应的化学方程式为:( CaCO3+2HCl═CaCl2+H2O+CO2↑)
| 实验顺序 | 加入稀盐酸的质量 | 剩余固体质量 |
| 第一次 | 5g | 1.315g |
| 第二次 | 5g | 0.63g |
| 第三次 | 5g | 0.3g |
| 第四次 | 5g | m |
| 第五次 | 5g | 0.3g |
(1)表中m的数据是
(2)该石灰石样品中含CaCO3的质量分数为多少?
(3)求2g石灰石完全反应后可生成多少g CO2?
【考点】根据化学反应方程式的计算.
【专题】综合计算(图像型、表格型、情景型计算题).
【分析】根据表中数据可以判断反应是否完全反应,并且能够判断m的值和碳酸钙的质量;
根据碳酸钙的质量可以计算生成二氧化碳的质量.
【解答】解:(1)第一次加入5g稀盐酸时,剩余固体质量是1.315g,反应的碳酸钙的质量为:2g﹣1.315g=0.685g,第二次加入5g稀盐酸时,剩余固体质量是0.63g,反应的碳酸钙的质量为:1.315g﹣0.63g=0.685g,第三次加入5g稀盐酸时,剩余固体质量是0.3g,反应的碳酸钙的质量为:0.63g﹣0.3g=0.33g,说明第三次加入稀盐酸时,碳酸钙已经完全反应,因此表中m的数据是0.3g.
故填:0.3.
(2)该石灰石样品中含CaCO3的质量分数为: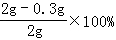 =85%
=85%
答:该石灰石样品中含CaCO3的质量分数为85%.
(3)设生成二氧化碳的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
2g﹣0.3g x
 ,
,
x=0.748g,
答:生成二氧化碳的质量是0.748g.
【点评】本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.