题目内容
等质量的下列物质在氧气中完全燃烧,耗氧量最大的是( )
| A、硫 | B、镁 | C、碳 | D、铁 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:本题是选择题,解题方法有多种,最传统比较麻烦的方法就是,设相同质量的物质后根据化学方程式计算出每项中消耗氧气的质量,然后进行比较即可.另一种较简单的方法就是设消耗相同质量的氧气所需物质多少,然后根据此比较相同质量的物质在氧气中完全燃烧消耗氧气多少.
解答:解:根据所该物质写出这4个反应的化学方程式,按O2的化学计量数为1进行配平;计算每种物质与O2的质量比,然后比较得出答案.
S+O2
SO2、2Mg+O2
2MgO C+O2
CO2、
Fe+O2
Fe3O4
32 32 48 32 12 32 84 32
消耗32份质量的O2所需4种物质的相对质量分别为:12、32、48、84,即消耗等量需要碳的质量最少.那么等质量的四种物质碳消耗的氧气的质量最大.
分析题给的选项可以知道选项C是正确的.
故选C.
S+O2
| ||
| ||
| ||
| 3 |
| 2 |
| ||
| 1 |
| 2 |
32 32 48 32 12 32 84 32
消耗32份质量的O2所需4种物质的相对质量分别为:12、32、48、84,即消耗等量需要碳的质量最少.那么等质量的四种物质碳消耗的氧气的质量最大.
分析题给的选项可以知道选项C是正确的.
故选C.
点评:解答该题的方法是很多种的,但是最简单的方法就是我们称之为“归一法”,即假定某种物质的化学计量数为“1”,或假定每种物质各1g,写出化学方程式,便可计算比较出结果.

练习册系列答案
相关题目
金属材料在生产、生活中有着重要意义.某同学在一次化学探究活动中,将甲、乙两种金属分别投入硫酸铜溶液中,发现甲的表面有红色物质析出,乙的表面没有明显现象.该同学对甲、乙和铜三种金属活动性大小的判断正确的是( )
| A、甲>铜>乙 |
| B、乙>铜>甲 |
| C、甲>乙>铜 |
| D、铜>甲>乙 |
空气的成分:①氮气,②氧气,③二氧化碳,④稀有气体.按体积分数计算,由多到少的顺序是( )
| A、②①③④ | B、①②③④ |
| C、④③②① | D、①②④③ |
有关溶液(溶质为固体)的说法中,正确的是( )
| A、饱和溶液降温后,一定有晶体析出 |
| B、凡是均一、透明的液体一定是溶液 |
| C、改变条件,饱和溶液与不饱和溶液可相互转化 |
| D、不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 |
在CuSO4中铜元素、硫元素、氧元素的质量比为( )
| A、2:1:2 |
| B、1:1:4 |
| C、4:2:1 |
| D、1:2:1 |
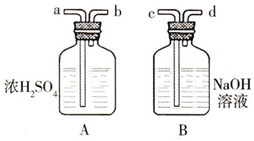 用锌粒和盐酸反应制取氢气,常混有水蒸气和氯化氢气体,为了获得纯净、干燥的氢气,可使混合气体通过如图所示的A、B两装置,气体通过两瓶的导管顺序正确的是( )
用锌粒和盐酸反应制取氢气,常混有水蒸气和氯化氢气体,为了获得纯净、干燥的氢气,可使混合气体通过如图所示的A、B两装置,气体通过两瓶的导管顺序正确的是( )| A、abcd | B、dcba |
| C、cdab | D、bacd |
生铁和稀盐酸充分反应后,过滤,留在滤纸上的物质是( )
| A、氯化亚铁 | B、铁 |
| C、碳和一些杂质 | D、氯化铁 |