题目内容
17.现有稀H2SO4、CuO、Fe粉3种物质,请设计两种制取铜的实验方案,填写如表:| 实验方案 | 有关反应的化学方程式 |
| 方案一 | (1)Fe+H2SO4=FeSO4+H2↑ (2)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O |
| 方案二 | (1)CuO+H2SO4=CuSO4+H2O (2)Fe+CuSO4=Cu+FeSO4 |
分析 根据题中所给反应物和要制备的物质分析反应原理.可得方案分别为:方案一:Fe $\stackrel{H_{2}SO_{4}}{→}$H2 $\stackrel{CuO}{→}$Cu
方案二:CuO $\stackrel{H_{2}SO_{4}}{→}$CuSO4 $\stackrel{Fe}{→}$Cu.
判断一个实验方案的好坏要从操作简便,结果明显,环保,节能等角度考虑.
解答 解:反应物有铁、硫酸、氧化铜,可以设计两种方案,①先用硫酸和铁制得氢气,再用氢气还原氧化铜制取铜,需要有制气装置和加热还原装置;②用氧化铜与硫酸反应制得硫酸铜,再用铁置换出硫酸铜中的铜,需要有反应装置和过滤装置,
故答案为:
| 实验方案 | 有关反应的化学方程式 |
| 方案一 | (1)Fe+H2SO4=FeSO4+H2↑ (2)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O |
| 方案二 | (1)CuO+H2SO4=CuSO4+H2O (2)Fe+CuSO4=Cu+FeSO4 |
点评 本题从化学方程式,实验方案的评价选择等方面进行了考查,综合性强,是一道很好的中考题.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
7.下列关于水的说法,错误的是( )
| A. | 水是一种常用的溶剂 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 明矾可促进水中悬浮杂质的沉降 | |
| D. | 长期饮用蒸馏水对人体健康非常有利 |
5.日常生活中的下列现象,属于缓慢氧化的是( )
| A. | 动植物的呼吸 | B. | 木炭燃烧 | C. | 火药爆炸 | D. | 铁丝燃烧 |
9.下列肥料属于复合肥的是( )
| A. | K2CO3 | B. | NH4HCO3 | C. | KNO3 | D. | Ca(H2PO4)2 |
7. 如图是钾元素在元素周期表中的部分信息及钾原子的原子结构示意图,根据图示判断下列表述正确的是( )
如图是钾元素在元素周期表中的部分信息及钾原子的原子结构示意图,根据图示判断下列表述正确的是( )
 如图是钾元素在元素周期表中的部分信息及钾原子的原子结构示意图,根据图示判断下列表述正确的是( )
如图是钾元素在元素周期表中的部分信息及钾原子的原子结构示意图,根据图示判断下列表述正确的是( )| A. | x=2 | B. | 钾元素属于非金属元素 | ||
| C. | 钾原子的质量为39.10g | D. | 钾原子的核电荷数为19 |
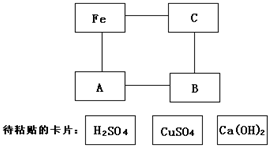 如图是化学园地中一张表示物质间反应关系的卡片图(“----”表示相连的两种物质能够在溶液体系中发生化学反应),其中A、B、C三处的卡片尚未粘贴.
如图是化学园地中一张表示物质间反应关系的卡片图(“----”表示相连的两种物质能够在溶液体系中发生化学反应),其中A、B、C三处的卡片尚未粘贴.