题目内容
4.有一部分变质的氢氧化钠固体,经测定其中含氢氧化钠80%,碳酸钠10.6%,其余为水.取该固体10g加水溶解后,向其中加入100g质量分数为14.6%的稀盐酸充分反应后,剩余的盐酸再用50g质量分数为14.4%的氢氧化钠溶液刚好完全中和.将反应后的溶液蒸发,可得到干燥固体多少克?分析 根据稀盐酸和氢氧化钠反应,以及与碳酸钠反应的方程式找到氯化氢生成氯化钠的质量关系,列比例式求解.
解答 解:
由反应的方程式:NaOH+HCl=NaCl+H2O;2HCl+Na2CO3=2NaCl+H2O+CO2↑
完全反应后生成溶质只有氯化钠,
设可得到干燥氯化钠固体质量为x.
可见氯化氢生成氯化钠的质量关系为:HCl~NaCl
36.5 58.5
100g×14.6% x
$\frac{36.5}{100g×14.6%}$=$\frac{58.5}{x}$
x=23.4g
答:得到干燥氯化钠固体质量23.4g.
点评 本题难度不是很大,主关键是氯化氢生成氯化钠的质量关系,培养学生分析问题的能力和解决问题的能力

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
14.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.下列关于此反应的认识正确的是( )
| 物 质 | X | Y | Z | W |
| 反应前的质量/g | 20 | m | 16 | 14 |
| 反应后的质量/g | 4 | 6 | 60 | 50 |
| A. | 参加反应的X与Y的质量比为1:4 | |
| B. | 若W为水,则X或Y必定为酸或碱 | |
| C. | m的数值为64 | |
| D. | 若X为化合物,Y为单质,则该反应一定为置换反应 |
15.根据图中的信息判断,下列说法正确的是( )
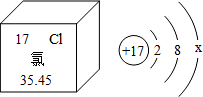

| A. | 氯原子的中子数是17 | B. | 氯原子核外有2个电子层 | ||
| C. | 当x=8时,该微粒是阳离子 | D. | 在化学变化中,氯原子易得到电子 |
12.X、Y、Z分别是NaOH、HCl、NaCl 中的一种溶液,将无色酚酞试液滴入Y,溶液变成红色,将此红色溶液少量滴加到X中红色褪去,则X、Y、Z依次是( )
| A. | NaOH、HCl、NaCl | B. | HCl、NaOH、NaCl | C. | NaCl、NaOH、HCl | D. | HCl、NaCl、NaOH |
16.如表对比实验(其他条件相同)能得到相应结论的是( )
| 选项 | 方 案 | 结 论 | |
| A |  | 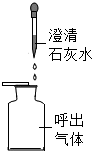 | 人呼出的气体全部是CO2 |
| B | 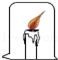 | 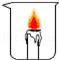 | 燃烧条件之一是可燃物的温度达到着火点 |
| C |  | 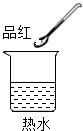 | 温度升高,分子运动加快 |
| D | 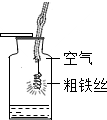 | 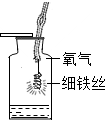 | 细铁丝与氧气反应比粗铁丝更激烈 |
| A. | A | B. | B | C. | C | D. | D |