题目内容
18.氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应,如图所示.
(1)硫在氧气中反应的现象为明亮的蓝紫色火焰、放出热量、生成有刺激性气味的气体,瓶中水的作用是吸收生成的二氧化硫,防止污染空气.
(2)如果按照图丙中所示进行铁丝在氧气中燃烧的实验,可能造成的后果是集气瓶壁炸裂.
(3)请从实验现象,反应类型两个角度说出图中三个反应的共同点:都放出热量、都属于化合反应.
(4)在做实验甲时,硫在氧气中燃烧比在空气中燃烧剧烈.做实验乙和丙时,木炭、铁丝在氧气中剧烈燃烧,而在空气中只是发红并未燃烧,据此,说明可燃物能否燃烧的剧烈程度与氧气的浓度(或氧气含量的多少)有关.
分析 氧气的化学性质是氧化性和助燃性,硫在纯氧中的现象是:明亮的蓝紫色火焰、放出热量、生成有刺激性气味的气体;瓶中水的作用是:吸收生成的二氧化硫,防止污染空气;如果按照图丙中所示进行铁丝在氧气中燃烧的实验,可能造成的后果是:集气瓶壁炸裂;从实验现象,反应类型两个角度说出图中三个反应的共同点:都放出热量;都属于化合反应;可燃物能否燃烧的剧烈程度与氧气的浓度或氧气含量的多少有关.
解答 解:(1)硫在纯氧中的现象是:明亮的蓝紫色火焰、放出热量、生成有刺激性气味的气体;瓶中水的作用是:吸收生成的二氧化硫,防止污染空气;故答案为:明亮的蓝紫色火焰、放出热量、生成有刺激性气味的气体;吸收生成的二氧化硫,防止污染空气;
(2)如果按照图丙中所示进行铁丝在氧气中燃烧的实验,可能造成的后果是:集气瓶壁炸裂;故答案为:集气瓶壁炸裂;
(3)从实验现象,反应类型两个角度说出图中三个反应的共同点:都放出热量;都属于化合反应;故答案为:都放出热量;都属于化合反应;
(4)可燃物能否燃烧的剧烈程度与氧气的浓度或氧气含量的多少有关;故答案为:氧气的浓度(或氧气含量的多少)
点评 本考点考查了考查了氧气的性质和物质燃烧的现象等,氧气有两个化学性质:氧化性和助燃性,氧气的化学性质也是中考的重要内容之一.同学们应该认真掌握,综合应用.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
6.下列化学方程式书写正确的是( )
| A. | 稀硫酸除铁锈:FeO+H2SO4═FeSO4+HO2 | |
| B. | 一氧化碳还原氧化铁Fe2O3+3CO═2Fe+3CO2↑ | |
| C. | 从废液中提取银:Zn+2AgNO3═Zn(NO3)2+2Ag | |
| D. | 加热氯化钾制取氧气:KClO3$\frac{\underline{\;\;△\;\;}}{\;}$KCl+O2↑ |
3.下列装置中不能用来测定空气中氧气含量的是( )
| A. | 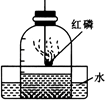 | B. | 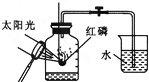 | C. |  | D. | 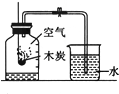 |

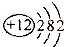 ,镁原子在化学反应中容易失去(填“得到”或“失去”)2个电子,形成的离子的符号是Mg2+,镁元素属于金属(填“金属”或“非金属”)元素.
,镁原子在化学反应中容易失去(填“得到”或“失去”)2个电子,形成的离子的符号是Mg2+,镁元素属于金属(填“金属”或“非金属”)元素.