题目内容
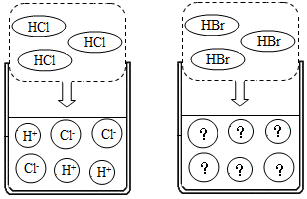
12.氢臭酸(HBr)的性质与盐酸非常相似.回答下列有关问题:(1)将紫色石蕊溶液滴入氢臭酸中,溶液将呈红色.
(2)HCl在水中的解离可表示为:HCl═H++Cl-,其解离过程为HBr═H++Br-.
(3)烧碱在空气中容易变质,变质反应的方程式为2NaOH+CO2=Na2CO3+H2O.若将氢臭酸滴入已经变质的烧碱溶液中,观察到有气泡现象产生,该过程中发生的化学方程式为Na2CO3+2HBr=2NaBr+H2O+CO2↑.
分析 (1)根据酸能使紫色石蕊试液变红色进行分析;
(2)根据氢溴酸在水中会解离出氢离子和溴离子进行分析;
(3)根据二氧化碳和氢氧化钠反应生成碳酸钠和水,碳酸钠和氢溴酸反应生成溴化钠、水和二氧化碳进行分析.
解答 解:(1)酸能使紫色石蕊试液变红色,所以将紫色石蕊溶液滴入氢臭酸中,溶液将呈红色;
(2)氢溴酸在水中会解离出氢离子和溴离子,所以解离过程为:HBr═H++Br-;
(3)二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O,碳酸钠和氢溴酸反应生成溴化钠、水和二氧化碳,化学方程式为:Na2CO3+2HBr=2NaBr+H2O+CO2↑.
故答案为:(1)红;
(2)HBr═H++Br-;
(3)2NaOH+CO2=Na2CO3+H2O,Na2CO3+2HBr=2NaBr+H2O+CO2↑.
点评 本题主要考查了利用类比思想解答问题的方法,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
11.如何保持良好的环境是当前我们面临的严峻挑战.下列行为,你认为正确的是( )
| A. | 将含富营养的生活废水排入湖泊以增加渔业的产量 | |
| B. | 鼓励多用电,促进电力事业的发展 | |
| C. | 大力发展公共交通,减少私家车的使用 | |
| D. | 减少绿地面积,扩大硬化场地以满足更多人的锻炼需求 |
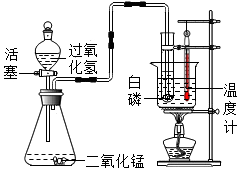 (1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;白磷未燃烧的原因是温度未达到白磷的着火点.
(1)当烧杯内的水受热,温度计显示30℃时,打开活塞,在盛有水的试管中有气泡均匀逸出,白磷未燃烧,关闭活塞.锥形瓶内反应的化学方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;白磷未燃烧的原因是温度未达到白磷的着火点.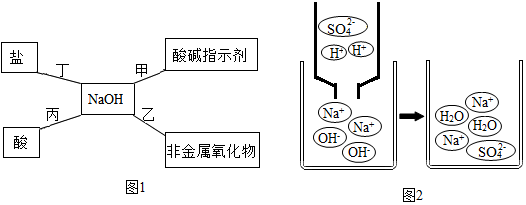
 将一根火柴折断,分成火柴头和火柴梗两部分,如图所示放在铜片上,用酒精灯加热铜片,观察到火柴头比火柴梗先燃烧.这说明火柴头的着火点比火柴梗的着火点低.火柴头上的深色物质主要含有氯酸钾,二氧化锰,硫磺和玻璃粉等,火柴梗上涂有少量石蜡,火柴盒两边的红褐色涂层是红磷和玻璃粉.划火柴时,借助摩擦放出氧气和热量,使可燃物燃烧.写出放出氧气的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
将一根火柴折断,分成火柴头和火柴梗两部分,如图所示放在铜片上,用酒精灯加热铜片,观察到火柴头比火柴梗先燃烧.这说明火柴头的着火点比火柴梗的着火点低.火柴头上的深色物质主要含有氯酸钾,二氧化锰,硫磺和玻璃粉等,火柴梗上涂有少量石蜡,火柴盒两边的红褐色涂层是红磷和玻璃粉.划火柴时,借助摩擦放出氧气和热量,使可燃物燃烧.写出放出氧气的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.