题目内容
9.某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,如果用双氧水和二氧化锰混合制氧气,为了得到平稳的氧气流,应该选A2(填序号).当产生的气体从B的左边导管通入时,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题:
(1)双氧水和二氧化锰混合制氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,B中白磷不燃烧,原因是温度没有达到白磷的着火点;
(2)C、D中看到的现象分别是C中液面下降,溶液被压入D中、溶液进入D中,D中固体逐渐减少,有无色气泡产生;
(3)E中颜色变化的原因二氧化碳和水反应生成了碳酸,碳酸能解离出氢离子,使石蕊变红,用F装置收集气体的依据是相同条件下,二氧化碳的密度大于空气,并且不与空气中的成分反应.
分析 根据注射器可以控制液体的滴加速度解答.
(1)由题意知,反应物双氧水,生成物水和氧气,反应条件为二氧化锰做催化剂,故可书写其化学方程式;根据燃烧的条件分析B中白磷不能够燃烧的原因;
(2)氧气流进入C,气压增大,则把盐酸压入D和石灰石反应生成二氧化碳;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;用F装置是向上排空气法,适合收集密度比空气大的气体.
解答 解:注射器可以控制液体的滴加速度,故了得到平稳的氧气流,应该选A2;
(1)由题意知,反应物双氧水,生成物水和氧气,反应条件为二氧化锰,故反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B中白磷没能够燃烧的原因是白磷虽然与氧气接触,但温度没有达到白磷的着火点;
(2)氧气流进入C,装置内的气压增大,则把盐酸压入D中和石灰石反应生成二氧化碳,因此观察到的现象是:C中液面下降;D中有液体进入且产生气泡;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;反应的化学方程式为:CO2+H2O=H2CO3;F装置收集气体是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大.
答案:
(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ 温度没有达到白磷的着火点
(2)C中液面下降,溶液被压入D中;溶液进入D中,D中固体逐渐减少,有无色气泡产生
(3)二氧化碳和水反应生成了碳酸,碳酸能解离出氢离子,使石蕊变红 相同条件下,二氧化碳的密度大于空气,并且不与空气中的成分反应
点评 本题是一道综合性的气体制取、收集、性质的考查,解决本题需要掌握氧气的反应原理、二氧化碳的实验室制法及其物理性质和化学性质及可燃物燃烧的条件等知识.

| A. | CO2气体(H2O)→生石灰 | B. | C粉(CuO)→稀盐酸 | ||
| C. | CaCl2溶液(HCl)→CaCO3粉末 | D. | CO气体(CO2)→NaOH溶液 |
| A. | 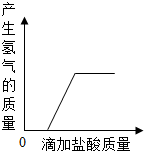 向一定质量表面生锈的铁片中滴加盐酸至过量 | |
| B. | 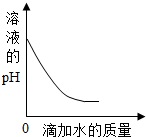 向一定质量稀硫酸中滴加水 | |
| C. | 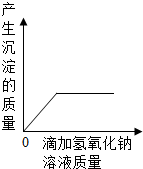 向FeCl3和HCl的混合溶液中滴加NaOH溶液至过量 | |
| D. |  高温煅烧一定质量的石灰石 |
| A. | 铁丝在氧气中剧烈燃烧、火星四射,生成白色固体 | |
| B. | 蜡烛在空气中和氧气中燃烧时火焰颜色相同 | |
| C. | 测定空气中氧气含量的实验里,铜粉加热变黑 | |
| D. | 木炭燃烧生成二氧化碳 |
 人类的日常生活和工农业生产离不开水.
人类的日常生活和工农业生产离不开水.(1)取2个烧杯,各盛大半烧杯浑浊的天然水,向其中1个烧杯中加入3药匙明矾粉末,搅拌溶解后,静置一段时间,观察到的现象是加过明矾的浑浊水样比未加的要澄清.
(2)如图所示,在电解器玻璃管内加满水,接通直流电源,一段时间后切断电源,用燃着的木条分别在两个玻璃管尖嘴口检验电解反应中产生的气体.完成下表:
| / | 气体体积 | 用燃着的木条检验气体时的现象 |
| 正极端玻璃管 | 5mL | 木条燃烧更旺 |
| 负极端玻璃管 | 10mL | 气体燃烧,产生淡蓝色火焰 |
| A. |  过滤 | B. |  蒸发食盐溶液 | C. |  点燃酒精灯 | D. |  滴加液体药品 |
 为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示:下列说法正确的是( )
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示:下列说法正确的是( )| A. | 图中表示化合物的是“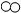 ” ” | |
| B. | 反应物与生成物均由分子构成 | |
| C. | 该反应中反应物两种分子的个数比为3:1 | |
| D. | 反应前后原子的种类和数目保持不变 |