��Ŀ����
12��2015��5��25�գ�����³ɽ�ص�һ�����꿵�����ķ������֣����38���������������˵����غ������1������Ա���ֳ����������в�����Ʒ���ٵ������ϴ������ڴ��������۴���ʯ����ȣ����������л��ϳɲ��ϵ��Ǣ٣�����ţ�����Ʒ�ٺ͢�Ϊȼ���ṩ�˿�ȼ���ȼ�յ���������
��2�������Ż�ʱ��ʹ�øɷ��������𣬸ɷ۵���Ҫ�ɷ���̼�����ƣ����Ⱥ�����̼���κ������������д���÷�Ӧ�Ļ�ѧ����ʽ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
���� ��1���л��ϳɲ��ϱ���߱�����������һ���л�������˹��ϳɣ����Ǹ߷��ӻ��������ȼ�յ������жϣ�
��2������̼���������ȷֽ�ķ�Ӧԭ�����ɣ�
��� �⣺��1���������ϴ������л��ϳɲ��ϣ�����������Ȼ���ϣ�����ʯ�����������Σ���ȼ�յ������������ٵ������ϴ������ڴ��������ڿ�ȼ�
��2��̼���������ȷֽ�ķ�Ӧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
�ʴ�Ϊ����1���٣���ȼ�2��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
���� �ϳɲ��ϵ�ʹ����Ҫ��ָ���ϡ��ϳ���ά���ϳ���������ϳɲ��ϣ����Ϸ�Ϊ�ϳɲ��ϡ��������ϡ����ǽ������Ϻ��ϲ��ϣ�

��ϰ��ϵ�д�
 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
�����Ŀ
2�����������ǻ�ѧѧϰ�����еij��÷���������������ȷ���ǣ�������
| A�� | ���ʺ����������ķ�Ӧ��������Ӧ�����Է���������Ӧһ���������μ� | |
| B�� | ���ӡ�ԭ�ӿ��Թ������ʣ���������һ�����ɷ��ӡ�ԭ�ӹ��ɵ� | |
| C�� | ��ȼ��ȼ��ʱ�¶���Ҫ�ﵽ�Ż�㣬���Կ�ȼ����¶ȴﵽ�Ż��һ����ȼ�� | |
| D�� | �������Ǻ��в�ͬԪ�صĴ�������Ժ��в�ͬ��Ԫ�صĴ�����һ���ǻ����� |
20�����б仯�У����������仯���ǣ�������
| A�� | ������ȼ | B�� | ��ѩ�ڻ� | C�� | ����ȼ�� | D�� | ��ʳ��� |
7�����������е��������ʣ�������Ϊ���ʣ���ֻ������NaOH�Ĺ������Һ���ܳ�ȥ���ǣ�������
| A�� | CO2��H2O�� | B�� | CO2��HCl�� | C�� | NaCl��Һ��MgCl2�� | D�� | KNO3��Һ��H2SO4�� |
17��ij��ȤС�鷢����һ�����ڷ��õļ�ʯ����Ʒ��Ϊ̽����ɷ֣�ͬѧ����ʵ���Ҷ������ʯ����Ʒչ����̽����
���������ϡ��ټ�ʯ������CaO��NaOH�����϶��ɣ�ͨ���������ն�����̼���������壮
����ʯ������ˮ��������ˮ�ų����������ٿ��Ժ��Բ��ƣ�
��BaCl2��Һ�����ԣ�
��������롿�������ϣ�ͬѧ�Ƿ�����ʯ����Ʒ����Ҫ�ɷֿ��ܺ���CaO��NaOH��Ca��OH��2��CaCO3��̼���ƣ�
��ʵ��̽����С�����ۺ��������ʵ�����̽����
��˼���������
С��ͬѧ����������Ϊ����ڵĽ��۲�ȷ��ԭ����Ca��OH��2+Na2CO3�TCaCO3��+2NaOH���û�ѧ����ʽ��ʾ����
����������ۡ�
ͨ������̽������������Եó��ü�ʯ����Ʒһ�����е�������Na2CO3��Ca��OH��2��ʵ��̽�������������Һ�г���̪����е�������NaOH��NaCl��BaCl2��
���������ϡ��ټ�ʯ������CaO��NaOH�����϶��ɣ�ͨ���������ն�����̼���������壮
����ʯ������ˮ��������ˮ�ų����������ٿ��Ժ��Բ��ƣ�
��BaCl2��Һ�����ԣ�
��������롿�������ϣ�ͬѧ�Ƿ�����ʯ����Ʒ����Ҫ�ɷֿ��ܺ���CaO��NaOH��Ca��OH��2��CaCO3��̼���ƣ�
��ʵ��̽����С�����ۺ��������ʵ�����̽����
| ʵ�鲽�輰���� | ʵ������ | ���� |
| ��ȡ���ָ���Ʒ���Թ��У�������ˮ | �����Է������� | ��ʯ����Ʒ�в���CaO�� �������� |
| �ڼ���������ˮ�������� | ������ɫ���� | ��Ʒ��һ������CaCO3 |
| �۴Ӳ���ڵ��Թ���ȡ�����ϲ���Һ����һ�Թ��У������еμӹ���BaCl2��Һ | ������ɫ���� | / |
| �ܽ�������������ʹ��ˣ�����Һ�еμ���ɫ��̪��Һ | ��Һ���ɫ |
С��ͬѧ����������Ϊ����ڵĽ��۲�ȷ��ԭ����Ca��OH��2+Na2CO3�TCaCO3��+2NaOH���û�ѧ����ʽ��ʾ����
����������ۡ�
ͨ������̽������������Եó��ü�ʯ����Ʒһ�����е�������Na2CO3��Ca��OH��2��ʵ��̽�������������Һ�г���̪����е�������NaOH��NaCl��BaCl2��
4�����һ���Ż���ʵ�鷽������֤ij�Ȼ�����Һ�л���̼���ơ������ƺ��������Ʋ��ᴿ�Ȼ��ƣ���ʵ�����̼�����ʵ��������ͼ��ʾ������˵������ȷ���ǣ�������
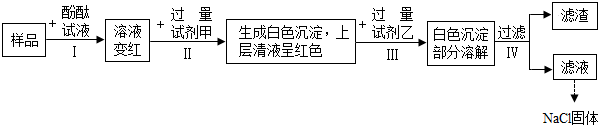

| A�� | ��Ʒ��Һ��pH����7 | |
| B�� | �Լ�����BaCl2��Һ | |
| C�� | �ڢ�ʵ���л��۲쵽�������������ݲ��� | |
| D�� | ���һ��������Һ���е�������NaCl��BaCl2��HCl��ָʾ�����⣩ |
3��NaOH��Na2CO3��NaCl�ڲ�ͬ�ܼ��е��ܽ�����±���ʾ��
��1 NaOH��Na2CO3��NaCl�ֱ���ˮ�е��ܽ�ȣ�S/g��
��2 �����£�NaOH��Na2CO3��NaCl�ֱ����Ҵ��е��ܽ�ȣ�S/g��
���ݱ�1�ͱ�2�ṩ�����ݻش��������⣺
��1��NaOH��ˮ�е��ܽ�����¶����߶����������С����
��2��20��ʱ������ʳ��ˮ�����ʵ���������Ϊ26.5%����������ȷ��0.1%����
��3��Ϊ֤��CO2����NaOH������Ӧ��С��ͬѧ��CO2ͨ�뱥��NaOH���Ҵ���Һ�У����Ʋ��ʵ��ɹ۲쵽��������Һ����ǣ��Ʋ�������̼�������Ҵ��е��ܽ�Ⱥ�С��
��1 NaOH��Na2CO3��NaCl�ֱ���ˮ�е��ܽ�ȣ�S/g��
| t/�� | NaOH | Na2CO3 | NaCl |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
| NaOH | Na2CO3 | NaCl |
| 17.3 | ��0.01 | 0.1 |
��1��NaOH��ˮ�е��ܽ�����¶����߶����������С����
��2��20��ʱ������ʳ��ˮ�����ʵ���������Ϊ26.5%����������ȷ��0.1%����
��3��Ϊ֤��CO2����NaOH������Ӧ��С��ͬѧ��CO2ͨ�뱥��NaOH���Ҵ���Һ�У����Ʋ��ʵ��ɹ۲쵽��������Һ����ǣ��Ʋ�������̼�������Ҵ��е��ܽ�Ⱥ�С��