题目内容
11. 请回答下列有关金属的问题.
请回答下列有关金属的问题.(1)铝是活泼金属,为什么通常铝锅却很耐腐蚀?
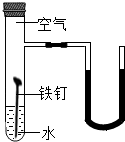
(2)如图是某探究实验装置图.一段时间后,能观察到什么现象?(装置气密性良好,且开始时U型管两端的红墨水液面相平)
(3)X、Y是两种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化,将X浸入硝酸银溶液中,X表面有银析出.
①判断X、Y和银三种金属的活动性由强到弱的顺序.
②具体确定一种X后,写出X与硝酸银溶液反应的化学方程式.
分析 (1)根据铝会与空气中的氧气生成致密的氧化铝薄膜进行分析;
(2)根据铁钉在潮湿的环境中易于氧气发生反应,从而使密封试管内的氧气密度与压强均发生了改变进行分析;
(3)根据金属活动性顺序,位于前面的金属会将位于后面的金属从其盐溶液中置换出来进行分析.
解答 解:(1)铝在空气中易与氧气反应生成致密的氧化膜,附着在铝的表面,阻止了反应的进一步进行;
(2)铁钉处在潮湿的空气中易生锈,消耗了密封试管内的氧气,使其压强减小,外界大气压不变,所以U型管右侧液面下降,左侧液面上升;
(3)①X、Y是两种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化,推知Y的活动性大于X的活动性,将X浸入硝酸银溶液中,X表面有银析出,推知X的活动性大于Ag,综上所述则有:Y>X>Ag;
②选用的X其活动性要排在H与Ag之间即可,如Cu、Hg等,则铜和硝酸银反应生成硝酸铜和银,化学方程式为:Cu+2AgN03=Cu(N03)2+2Ag;
故答案为:
(1)铝与氧气反应,其表面生成致密的氧化铝薄膜起保护作用;
(2)铁钉生锈,U型管液面变为左高右低;
(3)①Y>X>Ag;②Cu+2AgN03=Cu(N03)2+2Ag;
点评 本题综合考查的是金属的化学性质及其性质的应用和化学方程式的书写.

练习册系列答案
相关题目
1. 食醋是厨房中的一种调味品,其中含有少量醋酸,其分子结构如图,下列有关醋酸的说法不正确的是( )
食醋是厨房中的一种调味品,其中含有少量醋酸,其分子结构如图,下列有关醋酸的说法不正确的是( )
 食醋是厨房中的一种调味品,其中含有少量醋酸,其分子结构如图,下列有关醋酸的说法不正确的是( )
食醋是厨房中的一种调味品,其中含有少量醋酸,其分子结构如图,下列有关醋酸的说法不正确的是( )| A. | 醋酸分子是有碳、氢、氧三种原子构成的 | |
| B. | 醋酸中碳元素的质量分数为40% | |
| C. | 醋酸是由碳、氢、氧三个元素组成的 | |
| D. | 每个醋酸分子中含有8个原子核 |
2.上合组织成员国总理会议于2015年12月在郑州举行,会议期间各成员国总理们品尝了河南烩面、吊炉烧饼、铁棍山药等具有浓郁河南味地方特色的菜品.则“铁棍山药”中富含的淀粉属于下列哪种营养素( )
| A. | 糖类 | B. | 油脂 | C. | 维生素 | D. | 蛋白质 |
19. 甲、乙两种固体的溶解度曲线如下图所示.下列叙述正确的是( )
甲、乙两种固体的溶解度曲线如下图所示.下列叙述正确的是( )
 甲、乙两种固体的溶解度曲线如下图所示.下列叙述正确的是( )
甲、乙两种固体的溶解度曲线如下图所示.下列叙述正确的是( )| A. | t1℃时,甲和乙溶液中溶质的质量分数一定相等 | |
| B. | t2℃时,用等质量的甲和乙固体配制饱和溶液,得到乙饱和溶液的质量大于甲 | |
| C. | 将甲、乙的饱和溶液从t1℃升温至t2℃,甲溶液中溶质的质量分数比乙大 | |
| D. | 要想从乙的饱和溶液中得到晶体,最好用“冷却热饱和溶液”方法得到晶体 |
16.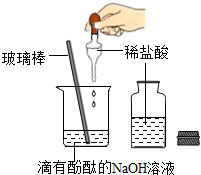 是酸碱中和反应的实验,下列操作中错误的是( )
是酸碱中和反应的实验,下列操作中错误的是( )
 是酸碱中和反应的实验,下列操作中错误的是( )
是酸碱中和反应的实验,下列操作中错误的是( )| A. | 打开细口瓶后,瓶盖倒放 | |
| B. | 用玻璃棒搅拌,使反应充分进行 | |
| C. | 烧杯可以作反应容器 | |
| D. | 取酚酞的胶头滴管,接着取细口瓶中的稀盐酸 |
3.下列化学方程式正确的是( )
| A. | KClO3$\frac{\underline{\;MnO_2\;}}{\;}$KCl+02↑ | B. | NaC03+HCl═NaCl+H20+C02↑ | ||
| C. | 2Ag+2HCl═2AgCl↓+H2↑ | D. | H2SO4+Cu(OH)2═CuS04+2H2O |
20.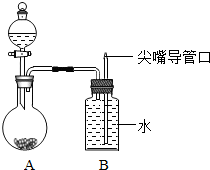 小明设计了趣味实验装置(见如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
小明设计了趣味实验装置(见如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
 小明设计了趣味实验装置(见如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )
小明设计了趣味实验装置(见如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )| A. | 氯化钠和水 | B. | 硝酸钠和水 | C. | 氢氧化钠和水 | D. | 铜和稀硫酸 |
1.下列安全标志中,表示“禁止燃放鞭炮”的是( )
| A. |  | B. |  | C. |  | D. |  |