题目内容
钢铁、铝合金、铜制品等是应用广泛的金属材料.据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一.某校化学兴趣小组的同学欲探究金属腐蚀的原因,设计了如下实验.
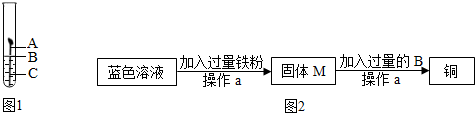
(1)如图1,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化.几天后,他们会发现 处最先出现铁锈,大家结合书本知识知道,铁在空气中生锈实际是铁和 、 等物质相互作用,发生一系列复杂的化学反应的过程.
(2)一位同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈.他们上网查阅资料,知道这种绿色物质的化学成分为Cu2(OH)2CO3(铜绿).他们根据铜绿组成和空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有 参加反应.
(3)向铜绿中加入适量稀硫酸,固体逐渐溶解,得到蓝色溶液,从蓝色溶液中回收铜的过程如图2:
①操作a的名称是 .用到的玻璃仪器有:玻璃棒、烧杯、 .
②证明B过量的现象是 .
③蓝色溶液加入过量铁粉发生反应的现象为 .
④防止金属锈蚀的方法很多,如制成不锈钢、在金属表面 (任写一种方法).

(1)如图1,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化.几天后,他们会发现
(2)一位同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈.他们上网查阅资料,知道这种绿色物质的化学成分为Cu2(OH)2CO3(铜绿).他们根据铜绿组成和空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有
(3)向铜绿中加入适量稀硫酸,固体逐渐溶解,得到蓝色溶液,从蓝色溶液中回收铜的过程如图2:
①操作a的名称是
②证明B过量的现象是
③蓝色溶液加入过量铁粉发生反应的现象为
④防止金属锈蚀的方法很多,如制成不锈钢、在金属表面
考点:金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)钢铁生锈的条件是钢铁与氧气和水同时接触,据此填空;
(2)根据铜绿中含有的元素来进行分析猜想;
(3)向铜锈中加入过量稀硫酸,固体逐渐溶解,得到蓝色溶液,由从蓝色溶液中回收铜的过程可知:
①得到蓝色溶液为硫酸铜和稀硫酸的混合液,加过量的铁粉时反应后所得为固体与溶液的混合物,故可知操作a的名称.
②依据B属于稀酸的实际,所以证明B过量方法是取滤液少量于试管中,向试管中加入少量锌粒,观察现象.
③蓝色溶液加入过量铁粉发生反应的化学方程式为:铁与硫酸和硫酸铜分别反应.
④根据铁锈蚀的条件来分析.
(2)根据铜绿中含有的元素来进行分析猜想;
(3)向铜锈中加入过量稀硫酸,固体逐渐溶解,得到蓝色溶液,由从蓝色溶液中回收铜的过程可知:
①得到蓝色溶液为硫酸铜和稀硫酸的混合液,加过量的铁粉时反应后所得为固体与溶液的混合物,故可知操作a的名称.
②依据B属于稀酸的实际,所以证明B过量方法是取滤液少量于试管中,向试管中加入少量锌粒,观察现象.
③蓝色溶液加入过量铁粉发生反应的化学方程式为:铁与硫酸和硫酸铜分别反应.
④根据铁锈蚀的条件来分析.
解答:解:(1)因为钢铁的锈蚀主要是铁与空气中的氧气、水蒸气等物质发生化学反应的结果,所以A、B、C三处中,B处先生锈;
(2)由铜绿的化学式Cu2(OH)2CO3可知,铜的锈蚀还可能与空气中的二氧化碳气体有关;
(3)①得到蓝色溶液为硫酸铜和稀硫酸的混合液,加入过量的铁粉,则铁能与稀硫酸反应,同时铁能置换出硫酸铜中的铜,所以反应后为铜铁的固体和硫酸亚铁的溶液,而操作a是分离固体与溶液的过程,所以是过滤;过滤需要用到的玻璃仪器主要有烧杯、玻璃棒和漏斗;
②固体M是铜与铁的混合物,分离两者时应加入稀硫酸或稀盐酸,所以证明B过量方法是:取滤液少量于试管中,向试管中加入少量锌粒,有气体产生,则证明B过量;
③蓝色溶液是硫酸铜与稀硫酸的混合物,所以加入过量铁粉发生反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑与Fe+CuSO4═FeSO4+Cu.故看到:蓝色溶液变成浅绿色,黑色粉末变成红色;
④铁与氧气、水接触时易发生锈蚀,所以可以在铁制品表面覆盖保护层,如刷漆等.
故答案为:(1)B;氧气;水蒸气;
(2)二氧化碳;
(3)①过滤; 漏斗; ②不再产生气体; ③蓝色溶液变成浅绿色,黑色粉末变成红色;④刷漆(答案合理即可).
(2)由铜绿的化学式Cu2(OH)2CO3可知,铜的锈蚀还可能与空气中的二氧化碳气体有关;
(3)①得到蓝色溶液为硫酸铜和稀硫酸的混合液,加入过量的铁粉,则铁能与稀硫酸反应,同时铁能置换出硫酸铜中的铜,所以反应后为铜铁的固体和硫酸亚铁的溶液,而操作a是分离固体与溶液的过程,所以是过滤;过滤需要用到的玻璃仪器主要有烧杯、玻璃棒和漏斗;
②固体M是铜与铁的混合物,分离两者时应加入稀硫酸或稀盐酸,所以证明B过量方法是:取滤液少量于试管中,向试管中加入少量锌粒,有气体产生,则证明B过量;
③蓝色溶液是硫酸铜与稀硫酸的混合物,所以加入过量铁粉发生反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑与Fe+CuSO4═FeSO4+Cu.故看到:蓝色溶液变成浅绿色,黑色粉末变成红色;
④铁与氧气、水接触时易发生锈蚀,所以可以在铁制品表面覆盖保护层,如刷漆等.
故答案为:(1)B;氧气;水蒸气;
(2)二氧化碳;
(3)①过滤; 漏斗; ②不再产生气体; ③蓝色溶液变成浅绿色,黑色粉末变成红色;④刷漆(答案合理即可).
点评:本题主要考查了常见金属的知识,熟练掌握有关铁、铜的知识,会分析、应用、解决一些具体问题是解题的关键.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
化学源于生活,同时又服务于生活.以下做法不合理的是( )
| A、食品包装充氮气以防腐 |
| B、乘坐公交车出行实现“低碳”生活 |
| C、用甲醛溶液浸泡海产品以保鲜 |
| D、用烧灼并闻气味的方法区别天然纤维和合成纤维 |
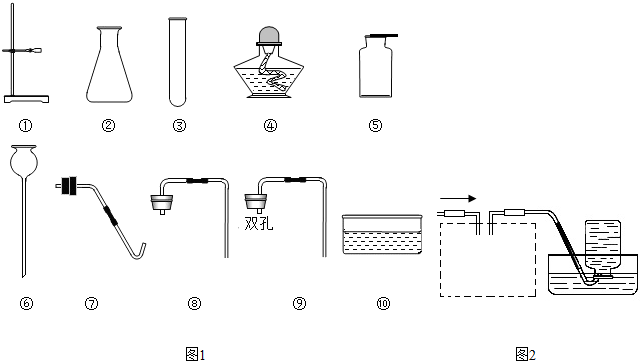
 碳酸钙是一种白色固体,可溶于稀盐酸并产生无色气体.某同学想知道稀盐酸中的那种 粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体.请你和同学们一起通过如图所示的四个实验完成这次探究活动.
碳酸钙是一种白色固体,可溶于稀盐酸并产生无色气体.某同学想知道稀盐酸中的那种 粒子(H2O、H+、Cl-)能使碳酸钙溶解并产生无色气体.请你和同学们一起通过如图所示的四个实验完成这次探究活动.
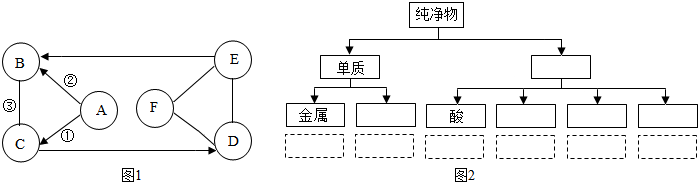
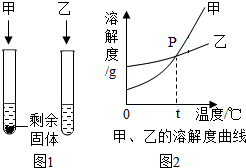 如图2为甲、乙两种固体物质在水中的溶解度曲线.
如图2为甲、乙两种固体物质在水中的溶解度曲线.