题目内容
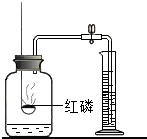
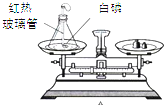 (1)某化学兴趣小组按照如图进行测定白磷燃烧后前后质量变化的实验探究,试回答下列问题:
(1)某化学兴趣小组按照如图进行测定白磷燃烧后前后质量变化的实验探究,试回答下列问题:①实验过程观察到的现象是:锥形瓶内有
②白磷燃烧的化学方程式为
(2)应用质量守恒定律进行判断:取A、B、C三种物质各20g,在一定条件下充分化合只能生成42g新物质D.若增加5gA,充分反应后原反应物中只有C剩余.下列说法正确的是
A.该反应是化合反应
B.第一次反应停止后,C剩余14g
C.反应中A和B的质量比是5:4
D.两次反应后,生成D的总质量为52.5g.
考点:质量守恒定律的实验探究,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据用白磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项进行分析;
(2)根据质量守恒定律指参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,而且两种物质每次参加反应的质量比是相等的进行分析.
(2)根据质量守恒定律指参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,而且两种物质每次参加反应的质量比是相等的进行分析.
解答:解:(1)①实验过程观察到的现象是:锥形瓶内有白烟产生;气球先胀大,后慢慢变得非常瘪.待白磷燃烧完毕,冷却后再称量,由于反应后锥形瓶内的物质既没有增多,有没有减少,因此天平的指针将会指向正中;若打开瓶塞后再称量,由于外界的空气进入锥形瓶中,使锥形瓶内的物质增多,因此天平的指针将会向左偏转;
②磷与氧气在点燃条件下反应生成五氧化二磷,化学方程式为:4P+5O2
2P2O5;
(2)根据题意可知:第二次增加5gA反应后只有C物质剩余,说明第一次反应后只有A物质20g完全反应,B、C都有剩余,又说明第二次反应后共用A物质25g,B物质20g,那么A物质两次反应的质量比为20g:25g=4:5.
A、反应物是三种,生成物是一种,所以该反应属于化合反应,故A正确;
B、设第一次反应用B物质质量为x,则有x:20g=4:5,解得x=16g,即第一次反应用B物质16g,那么第一次反应用C物质的质量为42g-20g-16g=6g,即第一次反应停止后C剩余20g-6g=14g,故B正确;
C、反应中A和B的质量比为25g:20g=5:4,故C正确;
D、设两次反应后,生成D的总质量为y,则有42g:y=4:5,解得y=52.5g,故D正确.
故答案为:(1)①大量白烟,气球先变大后缩小,正中,偏左;
②4P+5O2
2P2O5;
(2)ABCD.
②磷与氧气在点燃条件下反应生成五氧化二磷,化学方程式为:4P+5O2
| ||
(2)根据题意可知:第二次增加5gA反应后只有C物质剩余,说明第一次反应后只有A物质20g完全反应,B、C都有剩余,又说明第二次反应后共用A物质25g,B物质20g,那么A物质两次反应的质量比为20g:25g=4:5.
A、反应物是三种,生成物是一种,所以该反应属于化合反应,故A正确;
B、设第一次反应用B物质质量为x,则有x:20g=4:5,解得x=16g,即第一次反应用B物质16g,那么第一次反应用C物质的质量为42g-20g-16g=6g,即第一次反应停止后C剩余20g-6g=14g,故B正确;
C、反应中A和B的质量比为25g:20g=5:4,故C正确;
D、设两次反应后,生成D的总质量为y,则有42g:y=4:5,解得y=52.5g,故D正确.
故答案为:(1)①大量白烟,气球先变大后缩小,正中,偏左;
②4P+5O2
| ||
(2)ABCD.
点评:本题主要考查用白磷测定空气里氧气含量的实验和质量守恒定律的应用,难度较大.

练习册系列答案
相关题目
今年,会昌县委政府提出要“产业强县”,以下会昌产业生产过程主要涉及化学变化的是( )
| A、九二盐业真空制盐 |
| B、五丰公司米粉晾晒 |
| C、会昌国泰合成制药 |
| D、会昌石磊精选萤石 |
下列说法不正确的是( )
| A、物质都是由分子构成的 |
| B、同种分子化学性质相同 |
| C、分子是由原子构成的 |
| D、拍摄到苯分子图象说明分子是客观存在的 |