题目内容
1.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如表所示).他从瓶中倒出50毫升用于配制成稀硫酸,问:| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克•厘米-3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
(2)他将这50毫升浓硫酸与200克水均匀混合,求所得稀硫酸的质量分数.(结果保留一位小数)
(3)若实验室要配制630g溶质质量分数28%的稀硫酸,则需要这瓶溶质质量分数为98%的浓硫酸毫升?
分析 (1)根据m=ρV,溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
(3)根据溶液稀释前后,溶质的质量不变,结合密度公式进行分析解答.
解答 解:(1)50mL=50厘米3,m=ρV,这50毫升浓硫酸的质量是1.84克/厘米3×50厘米3=92g,其中含溶质的质量为92g×98%=90.16g;故填:92;90.16;
(2)溶液稀释前后溶质的质量不变,若将这50毫升浓硫酸与200克水均匀混合,所得稀硫酸的质量分数是$\frac{90.16g}{92g+200g}$×100%≈30.9%.故填:30.9%;
(3)设需要溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)的体积为x,
1.84g∕cm3×x×98%=630g×28% x≈97.8cm3=97.8mL.
答:需要溶质质量分数为98%的浓硫酸97.8毫升.
点评 本题难度不大,掌握溶质质量分数公式、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
11.下列各组物质的转化中,一定条件下均能一步实现的组合是( )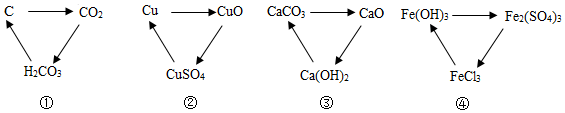

| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
9.(1)某实验小组利用如图实验装置探究二氧化碳的化学性质:
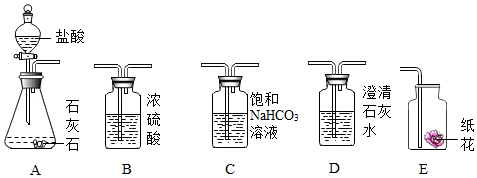
请根据实验装置和实验内容,回答下面问题:
①探究二氧化碳与碱反应时,将装置A生成的二氧化碳气体通入装置D未出现浑浊,原因是二氧化碳气体中混有氯化氢气体;可将二氧化碳先通过装置C,再通入装置D,理由是HCl+NaHCO3=NaCl+H2O+CO2↑(用化学方程式表示);
②探究二氧化碳与水反应时,实验分两步进行:首先将二氧化碳通过石蕊溶液浸泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目的是通过对比实验,证明二氧化碳和水反应生成碳酸,碳酸能使紫色变红色;结合上面实验,装置正确的连接顺序是ACBE(填序号)
(2)家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分是碳酸钠,可能含有少量氯化钠.小莉将家中食用碱带到实验室进行探究,请设计实验验证小莉提供的食用碱样品是否含有氯化钠.

请根据实验装置和实验内容,回答下面问题:
①探究二氧化碳与碱反应时,将装置A生成的二氧化碳气体通入装置D未出现浑浊,原因是二氧化碳气体中混有氯化氢气体;可将二氧化碳先通过装置C,再通入装置D,理由是HCl+NaHCO3=NaCl+H2O+CO2↑(用化学方程式表示);
②探究二氧化碳与水反应时,实验分两步进行:首先将二氧化碳通过石蕊溶液浸泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目的是通过对比实验,证明二氧化碳和水反应生成碳酸,碳酸能使紫色变红色;结合上面实验,装置正确的连接顺序是ACBE(填序号)
(2)家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分是碳酸钠,可能含有少量氯化钠.小莉将家中食用碱带到实验室进行探究,请设计实验验证小莉提供的食用碱样品是否含有氯化钠.
| 实验步骤 | 实验现象 | 结论与解释 |
| 1.取一定量的食用碱样品放入试管,加入蒸馏水、振荡 | 样品溶解 | 食用碱溶于水 |
| 2.向食用碱溶液的试管中,滴加几滴硝酸银溶液,振荡 | 有白色沉淀生成 | 还需要证明白色沉淀不溶于稀硝酸 |
| 3.向白色沉淀中滴加稀硝酸 | 沉淀不溶解 | 证明食用碱样品中含有氯化钠 |
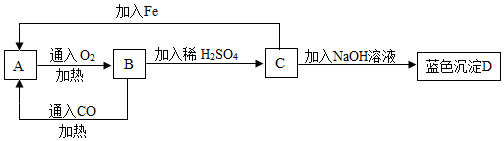
 已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连的物质可以发生反应,“→”表一种物质生成另一种物质(部分反应物、生成物及反应条件省略)
已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连的物质可以发生反应,“→”表一种物质生成另一种物质(部分反应物、生成物及反应条件省略)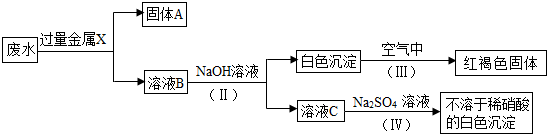
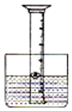 某化学兴趣小组,设计了如右图所示装置来研究空气中氧气的体积分数:用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升.向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.
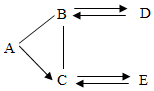
某化学兴趣小组,设计了如右图所示装置来研究空气中氧气的体积分数:用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升.向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.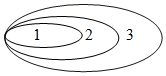 如果用如图表示各种概念之间的关系,下表选项中与图示不相符的是( )
如果用如图表示各种概念之间的关系,下表选项中与图示不相符的是( ) 


