题目内容
10.化学在交通、“节能减排”中发挥重要作用.(1)液化天然气(LNG)是我市正在推广的公交车燃料,它具有燃烧效率高、污染小的优点.写出天然气主要成分完全燃烧的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)汽车尾气中NO与CO在催化剂的作用下,反应生成CO2和一种无污染的单质气体.写出该反应的化学方程式:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
(3)氢化镁(MgH2)固体与水反应生成氢氧化镁和氢气,可为氢动力汽车提供能源.写出该反应的化学方程式:MgH2+2H2O═Mg(OH)2+2H2↑.
(4)我市倡导自行车“低碳出行”.采用碳纤维材料的自行车轻便、机械强度大,这应用了碳纤维的物理(填“物理”或“化学”)性质;自行车采用铝合金材料,金属铝具有较强抗腐蚀性的原因:表面容易生成一层致密的氧化物保护膜.
(5)为节约能源,使燃料充分燃烧,应考虑的因素是提供充足的氧气、增大接触面积.
分析 (1)天然气的主要成分是甲烷,甲烷燃烧生成水和二氧化碳;
(2)一氧化氮和一氧化碳在一定条件下反应生成二氧化碳和氮气;
(3)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(4)密度、机械强度等属于物质的物理性质;铝在通常情况下能被空气中的氧气氧化成一次致密的氧化物薄膜;
(5)根据使燃料充分燃烧的方法解答.
解答 解:
(1)天然气的主要成分是甲烷,完全燃烧生成了二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)NO与CO在催化剂的作用下,反应生成CO2和一种无污染的单质气体(由质量守恒定律,反应前后元素种类不变,该气体是氮气),反应的化学方程式为2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
(3)氢化镁(MgH2)固体与水反应生成氢氧化镁和氢气,该反应的化学方程式为:MgH2+2H2O═Mg(OH)2+2H2↑.
(4)采用碳纤维材料的自行车轻便、机械强度大,不需要发生化学变化就能表现出来,是利用了其物理性质.金属铝具有较强抗腐蚀性的原因是:表面容易生成一层致密的氧化物保护膜.
(5)为节约能源,使燃料充分燃烧,应考虑的因素是:提供充足的氧气、增大接触面积.
故答案为:
(1)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(2)2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2
(3)MgH2+2H2O═Mg(OH)2+2H2↑
(4)物理 表面容易生成一层致密的氧化物保护膜.
(5)提供充足的氧气、增大接触面积
点评 本题难度不大,主要考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

| A. | 铁在潮湿的空气中容易生锈 | |
| B. | 煤、石油和天然气是可再生能源 | |
| C. | 化肥碳酸氢铵(NH4HCO3)属于复合肥 | |
| D. | 催化剂在化学反应前后化学性质发生改变 |
| A. | 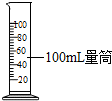 量取1mL水 | B. |  称取氯化钠 | C. | 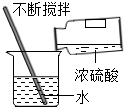 稀释浓硫酸 | D. | 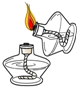 点燃酒精灯 |
| A. | 静置 | B. | 过滤 | C. | 吸附 | D. | 蒸馏 |
| 选项 | 物质 | 方法 |
| A | NaCl溶液(Na2SO4) | 加入过量的氯化钡溶液,过滤 |
| B | FeSO4溶液(CuSO4) | 加入过量的镁粉,过滤 |
| C | H2(HCl) | 依次通过盛有足量氢氧化钠溶液和浓硫酸的洗气瓶 |
| D | KCl(MnO2) | 加入足量的水,过滤,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 用肥皂水检验软水和硬水 | |
| B. | 用火柴检查天然气管道有无泄漏 | |
| C. | 冷碟子放在蜡烛火焰上方,得到炭黑 | |
| D. | 用灼烧的方法区别棉花和羊毛 |
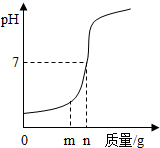 用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.
用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.