题目内容
每年的6月26日为世界禁毒日,罂粟碱是一种常见的毒品,其化学式为C19 H21O4N,下列关于罂粟碱的叙述正确的是( )
| A、罂粟碱是由碳、氢、氧、氮四个元素组成的化合物 |
| B、罂粟碱是由19个碳原子、21个氢原子、4个氧原子和1个氮原子构成的纯净物 |
| C、罂粟碱中碳、氧两种元素的质量比为19:4 |
| D、罂粟碱分子显电中性 |
考点:化学式的书写及意义,纯净物和混合物的判别,单质和化合物的判别,元素质量比的计算
专题:化学用语和质量守恒定律
分析:A、根据元素的宏观性质考虑;B、根据物质的分子的原子构成考虑;C、根据元素质量的计算方法考虑;D、根据分子的原子构成考虑.
解答:解:A、元素属于宏观概念,只讲种类不讲个数,所以元素不能说个数,故A错;
B、一个罂粟碱分子是由19个碳原子、21个氢原子、4个氧原子和1个氮原子构成的,解释分子才能用原子,故B错;
C、罂粟碱中碳、氧两种元素的质量比为:(12×19):(16×4)=57:16,故C错误;
D、罂粟碱分子是由原子构成,原子是由原子核和核外电子构成,原子核所带正电荷总数与核外电子所带负电荷总数相等,故原子不显电性,分子是由原子构成的,也不显电性,故D对.
故选C.
B、一个罂粟碱分子是由19个碳原子、21个氢原子、4个氧原子和1个氮原子构成的,解释分子才能用原子,故B错;
C、罂粟碱中碳、氧两种元素的质量比为:(12×19):(16×4)=57:16,故C错误;
D、罂粟碱分子是由原子构成,原子是由原子核和核外电子构成,原子核所带正电荷总数与核外电子所带负电荷总数相等,故原子不显电性,分子是由原子构成的,也不显电性,故D对.
故选C.
点评:解答本题关键是要知道元素的特点,物质的元素组成,分子的原子构成和元素质量的计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
现有镁、铝两种金属分别与稀盐酸充分反应,生成相同质量的氢气,则可能的情况有( )
| A、等质量的镁、铝分别与足量的稀盐酸充分反应 |
| B、质量比为4:3的镁、铝分别与足量的稀盐酸充分反应 |
| C、质量比为8:9的镁、铝分别与足量的稀盐酸充分反应 |
| D、足量的镁、铝分别与等质量、等浓度的稀盐酸充分反应 |
下列对高锰酸钾制取氧气时的“先”与“后”关系的描述中正确的是( )
| A、检查装置气密性,先把手掌紧贴容器外壁,再把导管伸入水中 |
| B、加热时,先对试管预热,再对准药品部位加热 |
| C、在装配仪器时,先装药品,再检查装置气密性 |
| D、收集气体结束时,先熄灭酒精灯,再把导管移出水面 |
“西气东输”工程中的“气”是指天然气,其主要成分是甲烷(CH4).下列有关“CH4”意义的认识不正确的是( )

| A、表示甲烷这种物质 |
| B、表示甲烷气体由1个碳原子和4个氢原子组成 |
| C、表示甲烷由碳、氢两种元素组成 |
| D、表示一个甲烷分子 |
我国最近已研究出新型水处理剂C1O2的新制法,其反应的微观过程如图所示.下列说法正确的是( )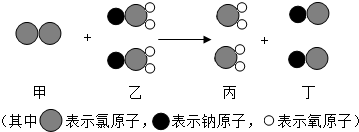

| A、乙中氯元素的化合价为+5价 |
| B、该反应属于分解反应 |
| C、该反应符合质量守恒定律 |
| D、该反应的化学方程式为2Cl+NaClO2═2ClO2+2NaCl |
下列过程主要发生化学变化的是( )
| A、酒精 醋酸汽油等物质挥发出气体分子 |
| B、二氧化碳在自然界的生态循环 |
| C、工业上由液态空气制得氧气 |
| D、晾晒的大头菜上出现白色物质 |
江苏省疾病预防控制中心专家指出,H7N9禽流感病毒和其它流感病毒一样,普通消毒剂很容易将其杀灭.戊二醛(C5H8O2)是一种高效消毒剂,下列有关戊二醛的说法不正确的是( )
| A、戊二醛属于有机高分子化合物 |
| B、戊二醛由碳、氢、氧三种元素组成 |
| C、戊二醛中碳、氢、氧的原子个数比为5:8:2 |
| D、20%的戊二醛溶液中氢元素的质量分数为1.6% |