题目内容
3.一定质量的氯酸钾与二氧化锰的混合物,加热一段时间后,二氧化锰的含量由a%增加到b%,则产生的氧气占原混合物质量百分比为( )| A. | (1-$\frac{b}{a}$)×100% | B. | (1-$\frac{a}{b}$)×100% | C. | (1+$\frac{b}{a}$)×100% | D. | (1+$\frac{a}{b}$)×100% |
分析 反应中二氧化锰是催化剂,反应前后质量不变,利用反应前后固体混合物中二氧化锰的质量分数,求得反应一段时间后生成氧气的质量.
解答 解:设原混合物的质量为w,产生氧气的质量为x
则加热前二氧化锰的含量:w×a%,
则加热后二氧化锰的含量:(w-x)×b%,
反应中二氧化锰是催化剂,反应前后质量不变,所以w×a%=(w-x)×b%
解得:x=$\frac{wb%-wa%}{b%}$=(1-$\frac{a}{b}$)×w
则产生的氧气占原混合物质量百分比为$\frac{(1-\frac{a}{b})×w}{w}$×100%=(1-$\frac{a}{b}$)×100%
故选B.
点评 利用催化剂在反应前后质量不变,由二氧化锰的质量计算出反应后固体的质量,此为解答本题的关键.

练习册系列答案
相关题目
13.下列关于氧气的说法,错误的是( )
| A. | 用含有氧元素的物质反应才有可能产生氧气 | |
| B. | 鱼、虾等能在水中生存,是由于氧气不易溶于水 | |
| C. | 红磷在氧气中燃烧产生大量白烟 | |
| D. | 用嘴吹灭蜡烛,利用的主要灭火原理是隔绝氧气 |
11.最近某些国家的科技人员研制出自动灭火砖.这种砖砌成的房屋发生火灾时,在高温烘烧下,砖会裂开喷出二氧化碳,从而扑灭火焰.自动灭火转的主要灭火原理是( )
| A. | 移走可燃物 | B. | 降低可燃物的着火点 | ||
| C. | 使可燃物与氧气隔绝 | D. | 使可燃物的温度降到着火点以下 |
18.某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
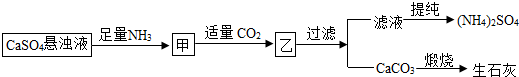
下列推断不合理的是( )

下列推断不合理的是( )
| A. | 该工艺流程没有消耗能源 | |
| B. | 煅烧CaCO3生成可CO2被循环使用 | |
| C. | 过滤操作用到了三种玻璃仪器 | |
| D. | 农业上过量使用(NH4)2SO4会造成土壤酸化 |
8.反应前密闭容器分别含有甲、乙、丙、丁、戊5种物质各10克,充分反应后,测得各物质的质量如表,则下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 反应后的质量/克 | 26 | 10 | 0 | 待测 | 4 |
| A. | 参加反应的物质质量比为5:2 | B. | 乙是反应的催化剂 | ||
| C. | 反应后生成甲物质26g | D. | 该反应属于化合反应 |
12.只用一种试剂就能鉴别NaCl、NH4Cl、Na2CO3三种溶液,该试剂是( )
| A. | NaOH溶液 | B. | Ca(OH)2溶液 | C. | KCl溶液 | D. | NaNO3溶液 |
13.分类是化学学习和研究的重要方法之一,下列分类方法中正确的是( )
| A. | 干冰、水、生石灰都是氧化物 | B. | 水银、碘酒、天然气都是混合物 | ||
| C. | 纯碱、烧碱、熟石灰都是碱 | D. | 葡萄糖、淀粉、碳酸钙都是有机物 |
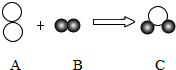 如图是用来表示某物质发生化学变化的微观示意图.图中○和●分别表示两种元素的原子,仔细观察下图,回答下列问题:
如图是用来表示某物质发生化学变化的微观示意图.图中○和●分别表示两种元素的原子,仔细观察下图,回答下列问题: