题目内容
16.瓦斯气是煤矿中多种气体的总称,但其主要气体X是一种常见化合物,该气体燃烧或发生爆炸反应的化学方程式可表示为:X+2O2═CO2+2H2O(1)瓦斯气中主要气体X的化学式为CH4.
(2)现有160gX与足量的氧气点燃后发生反应,可以生成二氧化碳的质量是多少?
分析 (1)根据化学反应前后原子的种类和数目不变进行解答;
(2)根据写出甲烷燃烧的化学方程式,根据甲烷的质量即可求出生成二氧化碳的质量.
解答 解:
(1)由化学反应前后原子的种类和数目不变和X+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O可知,X的化学式为CH4;
(2)设生成二氧化碳的质量为x
CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
16 44
160g x
$\frac{16}{160g}=\frac{44}{x}$
x=440g
答案:
(1)CH4;
(2)可以生成二氧化碳的质量是440g
点评 本题难度不大,主要考查了根据化学方程式计算有关的量,培养学生根据化学方程式计算的能力.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 空气中氮气的体积分数为21% | |
| B. | 测量空气中氧气的含量时,开始时未夹紧弹簧夹,会造成进水偏少 | |
| C. | 海洋中含量最多的非金属元素是氢元素 | |
| D. | 测量空气中氧气的含量时,塞子未塞紧,会造成进水偏少 |
1.下列溶液中PH最小的是( )
| A. | 使紫色石蕊变红的溶液 | B. | 不能使紫色石蕊变色的溶液 | ||
| C. | 使紫色石蕊变蓝的溶液 | D. | 使无色酚酞变红的溶液 |
8.下列反应既是氧化反应又是化合反应的是( )
| A. | 2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$ 2MgO | B. | 2H2O2=2H2O+O2↑ | ||
| C. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | D. | NaOH+HCl=NaCl+H2O |
5.取两份等质量的xCuCO3•yCu(OH)2固体,在一份中加入过量盐酸,生成CO28.8g;加热另一份使其完全分解,得到CuO40.0g.则x和y的关系正确的是( )
| A. | x:y=1:1 | B. | x:y=2:3 | C. | x:y=3:2 | D. | x:y=2:1 |
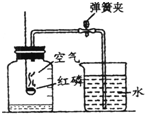 如图是顿珠同学用红磷在空气中燃烧的方法测定空气的成分,回答下列问题:
如图是顿珠同学用红磷在空气中燃烧的方法测定空气的成分,回答下列问题: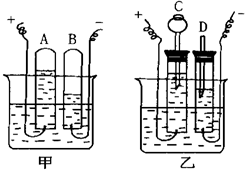 甲、乙两图都是电解水的简易装置.请你回答下列问题.
甲、乙两图都是电解水的简易装置.请你回答下列问题.