题目内容
【题目】碳和碳的化合物是初中学习的重要内容。
(1)金刚石、石墨和C60都是碳元素的单质,下列说法正确的是(填字母代号)_____。
A 它们都是同种物质 B 它们的原子排列方式不同
C 它们都能导电 D 常温下它们都能与氧气反应
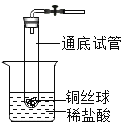
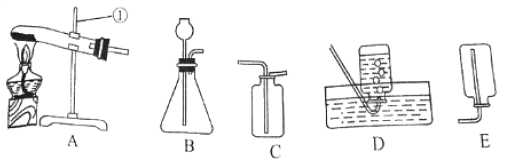
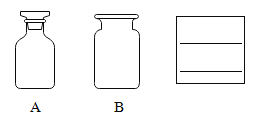
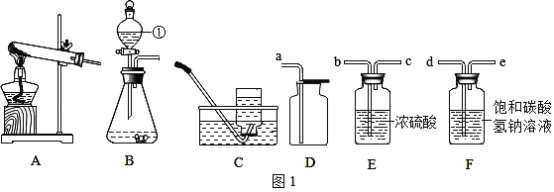
(2)实验室制取二氧化碳的原理是(用化学方程式表示)_____;若要得到干燥、纯净的二氧化碳,则发生装置产生的二氧化碳按气流方向连接顺序为(填导管接口字母):CO2→_____→_____→_____→_____→_____。
(3)实验结束后装置B锥形瓶中废液中溶质的成分是什么?
(猜想与假设)猜想一:CaCl2
猜想二:CaCl2、HCl;
猜想三:CaCl2、HCl、CaCO3. 该同学认为猜想三是错误的,理由是_____。
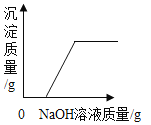
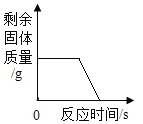
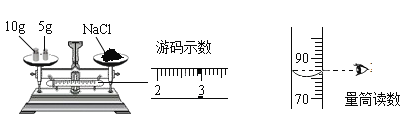
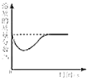
(实验验证)同学们对猜想与假设进行验证,取装置B锥形瓶中的废液过滤,向滤液中逐滴加入碳酸钠溶液,根据反应现象得到如图2所示的图象。
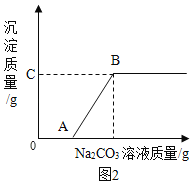
(结论)分析图象数据得出A点溶液的 pH=7,则废液中含有的阳离子有_____。OA段发生的反应为_____(用化学方程式表示),AB段溶液的pH_____(填“变大”“不变”或“变小”)。
(4)现取含碳酸钙80%的石灰石 12.5g和94.4g稀盐酸恰好完全反应(石灰石中的杂质不溶于水也不与稀盐酸反应),求恰好完全反应后所得溶液中溶质的质量分数_____。
【答案】B CaCO3+2HCl═CaCl2+H2O+CO2↑ d e b c a 碳酸钙和盐酸不能共存 钙离子、钠离子 Na2CO3+2HCl═2NaCl+H2O+CO2↑ 不变 11.1%
【解析】
(1)A.它们是不同种物质,该选项说法不正确;
B.它们的原子排列方式不同,该选项说法正确;
C.金刚石不能导电,石墨能够导电,该选项说法不正确;
D.常温下它们都不能与氧气反应,该选项说法不正确。
故填:B。
(2)实验室制取二氧化碳的原理是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;
若要得到干燥、纯净的二氧化碳,则发生装置产生的二氧化碳按气流方向连接顺序为(填导管接口字母):CO2→d→e→b→c→a。
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;d;e;b;c;a。
(3)[猜想与假设]
猜想一:碳酸钙和盐酸恰好完全反应时是CaCl2
猜想二:硬水过量时是CaCl2、HCl;
猜想三:CaCl2、HCl、CaCO3。
该同学认为猜想三是错误的,理由是碳酸钙和盐酸不能共存。
故填:碳酸钙和盐酸不能共存。
[结论]
分析图象数据得出A点溶液的 pH=7,即OA段是碳酸钠和稀盐酸反应,则废液中含有的阳离子有钙离子、钠离子;
OA段碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
AB段是碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,溶液的pH不变。
故填:钙离子、钠离子;Na2CO3+2HCl═2NaCl+H2O+CO2↑;不变。
(4)设反应生成氯化钙质量为x,生成二氧化碳质量为y,
碳酸钙质量:12.5g×80%=10g,
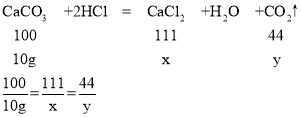
x=11.1g,y=4.4g,
恰好完全反应后所得溶液中溶质的质量分数:![]() ×100%=11.1%,
×100%=11.1%,
答:恰好完全反应后所得溶液中溶质的质量分数为11.1%。
故填:11.1%。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案