题目内容
①小新用在空气中燃烧镁带的实验来探究质量守恒定律:完全燃烧后,称量留下固体的质量比反应前镁带的质量还轻,联系实验过程分析,其原因可能有: ;
②已知铜在空气中生锈为Cu2(OH)2CO3,试写出同生锈的化学方程式: .
②已知铜在空气中生锈为Cu2(OH)2CO3,试写出同生锈的化学方程式:
考点:质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)验证质量守恒定律,关键是必须保证物质不和外界交换,要从实验条件及实验过程角度来分析.
(2)根据反应物和生成物及其质量守恒定律可以正确地书写化学方程式.
(2)根据反应物和生成物及其质量守恒定律可以正确地书写化学方程式.
解答:解:(1)首先本实验是在空气中进行的,镁燃烧时的现象为发出耀眼的白光并有白烟生成,白烟是氧化镁固体小颗粒,这一部分扩散到空气中.其次做实验时镁带要用坩埚钳夹住进行实验,所以燃烧后的白色粉末可能粘在坩埚钳上,导致质量减轻.
(2)铜和水、氧气、二氧化碳反应生成碱式碳酸铜,故反应的化学方程式为:2Cu+O2+H20+CO2=Cu2(OH)2CO3.
故答案为:(1)镁带燃烧时有一缕白烟(为生成的氧化镁)向空气中扩散,造成氧化镁的损失;镁带燃烧时夹镁带的坩埚钳上有-层白色粉末,此粉末为氧化镁,也造成氧化镁的损失.
(2)2Cu+O2+H20+CO2=Cu2(OH)2CO3.
(2)铜和水、氧气、二氧化碳反应生成碱式碳酸铜,故反应的化学方程式为:2Cu+O2+H20+CO2=Cu2(OH)2CO3.
故答案为:(1)镁带燃烧时有一缕白烟(为生成的氧化镁)向空气中扩散,造成氧化镁的损失;镁带燃烧时夹镁带的坩埚钳上有-层白色粉末,此粉末为氧化镁,也造成氧化镁的损失.
(2)2Cu+O2+H20+CO2=Cu2(OH)2CO3.
点评:验证质量守恒定律,条件的控制是关键,一般用密闭容器进行实验,称量前后容器的质量变化.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
氯气和氧气都是活泼的非金属单质,在一定条件下它们都能跟甲烷起反应.已知O2与CH4充分反应后的生成物是CO2和H2O,据此推知,Cl2与CH4反应后的生成物是( )
| A、CCl4和HCl |
| B、CCl4和Cl2 |
| C、CH2Cl2和HCl |
| D、CCl4和H2 |
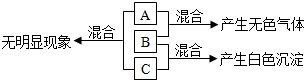
 某科技小组制作的一只喷气船模型如图所示,将船浮在室内游泳池的水面上,打开漏斗的活塞,流下的盐酸与碳酸钠反应产生大量的二氧化碳气体,塑料罐内气体迅速增多,压强增大,气体从罐底小孔喷出,使船前进.请回答下列问题:
某科技小组制作的一只喷气船模型如图所示,将船浮在室内游泳池的水面上,打开漏斗的活塞,流下的盐酸与碳酸钠反应产生大量的二氧化碳气体,塑料罐内气体迅速增多,压强增大,气体从罐底小孔喷出,使船前进.请回答下列问题: 如图是A、B两种物质的溶解度曲线.请下列各题.
如图是A、B两种物质的溶解度曲线.请下列各题.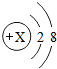 如图是某粒子的结构示意图,
如图是某粒子的结构示意图,