题目内容
12.高铁酸钠(Na2FeO4)是一种性能优良的净水剂.下列有关高铁酸钠的说法正确的是( )| A. | 属于氧化物 | |
| B. | 由两个金属元素和一个非金属元素组成 | |
| C. | 铁元素化合价为+6 | |
| D. | 其中钠、铁、氧元素质量比是2:1:4 |
分析 A.氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B.根据元素的规定来分析.
C.根据化合物中元素化合价的计算方法来分析解答.
D.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:A.高铁酸钠是由钠、铁、氧三种元素组成的化合物,属于氧化物,故选项说法错误.
B.元素是个宏观概念,只讲种类、不讲个数,故选项说法错误.
C.化合物中个元素化合价代数和为零,则有(+1)×2+铁的化合价+(-2)×4=0,即铁的化合价是+6价,故选项说法正确.
D.钠、铁、氧三种元素质量比是(23×2):56:(16×4)≠2:1:4,故选项说法错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
15.倡导科学生活,提高健康水平.下列做法正确的是( )
| A. | 发霉的大米蒸煮后食用 | |
| B. | 我们不要喝含汞、铅超标的水 | |
| C. | 用福尔马林保存海鲜 | |
| D. | 对于人体必需的元素摄入量越多越好 |
7.下列实验操作中,正确的是( )
| A. | 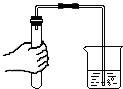 检查装置的气密性 | B. | 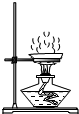 蒸发食盐水 | ||
| C. | 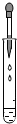 向试管中滴加液体 | D. | 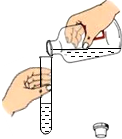 倾倒液体 |
4.金属铝及其合金有广泛的用途.
(1)请画出铝的原子结构示意图;
(2)铝的化学性质活泼却耐腐蚀的原因;
(3)铝是两性金属,既可以与酸溶液反应,也可以与碱溶液反应,与NaOH溶液反应生成NaAlO2和H2.写出化学反应方程式;
(4)Al在高温条件下可以与Fe3O4发生置换反应,得到Fe与另一种氧化物,写出化学方程式;
(5)实验室制取某气体所需装置如图所示:
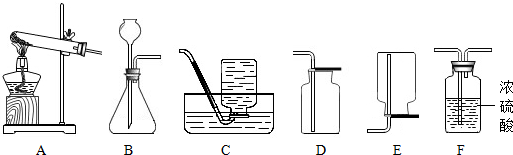
现欲制取一瓶干燥的H2,可选用图中的BFE组合制得.此操作中的发生装置还可以制取少量的另一种气体,请你写出产生另一种气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前都要检查装置的气密性,请在图中选择一个气体发生装置,简述其气密性的检验方法先从长颈漏斗中注入水,当水浸没其下端管口时,用止水夹夹住导气管上连接的胶皮管,保证此处不漏气;然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好.
(6)合金的用途十分广泛.某化学小组欲测定黄铜片(铜锌合金)的组成,进行了如下实验:取黄铜片30g放入烧杯中,将100g稀硫酸分5次加入烧杯中,每次均充分反应后,测得剩余固体的质量记录如表.
请计算:稀硫酸中溶质的质量分数.
(1)请画出铝的原子结构示意图;
(2)铝的化学性质活泼却耐腐蚀的原因;
(3)铝是两性金属,既可以与酸溶液反应,也可以与碱溶液反应,与NaOH溶液反应生成NaAlO2和H2.写出化学反应方程式;
(4)Al在高温条件下可以与Fe3O4发生置换反应,得到Fe与另一种氧化物,写出化学方程式;
(5)实验室制取某气体所需装置如图所示:

现欲制取一瓶干燥的H2,可选用图中的BFE组合制得.此操作中的发生装置还可以制取少量的另一种气体,请你写出产生另一种气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前都要检查装置的气密性,请在图中选择一个气体发生装置,简述其气密性的检验方法先从长颈漏斗中注入水,当水浸没其下端管口时,用止水夹夹住导气管上连接的胶皮管,保证此处不漏气;然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好.
(6)合金的用途十分广泛.某化学小组欲测定黄铜片(铜锌合金)的组成,进行了如下实验:取黄铜片30g放入烧杯中,将100g稀硫酸分5次加入烧杯中,每次均充分反应后,测得剩余固体的质量记录如表.
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 20 | 20 | 20 | 20 | 20 |
| 剩余固体质量/g | 26.75 | 23.5 | 20.25 | 17 | 16.5 |
2.下列试剂不能区分稀盐酸和澄清石灰水的是( )
| A. | 肥皂水 | B. | 紫色石蕊溶液 | C. | 食盐水 | D. | 碳酸钠溶液 |
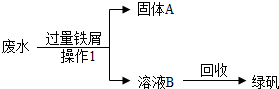 某工厂排出的废水中含有硫酸、硫酸铜,小艳同学取水样后进行研究性学习,请回答下列问题:
某工厂排出的废水中含有硫酸、硫酸铜,小艳同学取水样后进行研究性学习,请回答下列问题: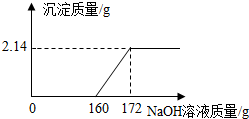 工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与NaOH反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与NaOH反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
