题目内容
7. 镁带在空气中放置一段时间表面会氧化,其中所含的其它杂质与稀硫酸不反应.为了测定某种镁带中镁的质量分数,某实验小组进行如下实验:先用细砂纸打磨镁带表面,使用精密天平称取打磨后11.25克镁带样品放在烧杯中,每次加入40.00克稀硫酸(不考虑水的挥发)使充分反应,测量反应前后装置连同内盛物质的质量.
镁带在空气中放置一段时间表面会氧化,其中所含的其它杂质与稀硫酸不反应.为了测定某种镁带中镁的质量分数,某实验小组进行如下实验:先用细砂纸打磨镁带表面,使用精密天平称取打磨后11.25克镁带样品放在烧杯中,每次加入40.00克稀硫酸(不考虑水的挥发)使充分反应,测量反应前后装置连同内盛物质的质量.记录实验数据如表:
| 加入稀硫酸次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯和所称物质总质量(克) | 120.15 | 159.95 | 199.75 | 239.55 | 279.45 | 319.45 |
(1)稀硫酸中溶质的质量分数.
(2)镁带样品中镁的质量分数.
(3)在坐标纸上绘出产生的气体质量与所加硫酸质量的关系曲线.
分析 根据表中提供的数据可以判断样品和稀硫酸反应的进行情况;
根据生成氢气的质量可以计算镁的质量,进一步可以计算样品中镁的质量分数;
根据提供的数据可以判断加入稀硫酸的质量与生成气体的质量关系.
解答 解:根据第1、2、3、4次实验数据可知,每加入40g稀硫酸可以产生0.2g氢气,第5次加入40g稀硫酸只产生0.1g氢气,说明镁已经反应完,共产生0.2g×4+0.1g=0.9g;
设稀硫酸中溶质的质量为x
Mg+H2SO4═MgSO4+H2↑,
98 2
x 0.2g
$\frac{98}{x}=\frac{2}{0.2g}$
x=9.8g
稀硫酸中溶质的质量分数=$\frac{9.8g}{40g}×$100%=24.5%
(2)设镁的质量为y,
Mg+H2SO4═MgSO4+H2↑,
24 2
y 0.9g
$\frac{24}{y}=\frac{2}{0.9g}$
y=10.8g
镁带样品中镁的质量分数=$\frac{10.8g}{11.25g}×$100%=96%
(3)产生的气体质量与所加硫酸质量的关系曲线如图: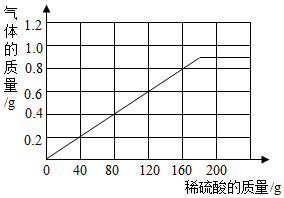
答案:
(1)稀硫酸中溶质的质量分数为24.5%;
(2)镁带样品中镁的质量分数为96%;
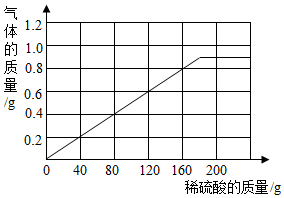
(3)
点评 本题主要考查学生化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.已知在相同的温度和压强下,任何气体的体积和分子数成正比.在1体积空气中混入1体积二氧化碳,在高温下跟足量的焦炭反应,假设氧气和二氧化碳都转化为一氧化碳,则反应后气体中一氧化碳的体积百分含量约是( )
| A. | 75% | B. | 50% | C. | 67% | D. | 33.3% |
2.下列物质能在pH=13的无色溶液中大量共存的是( )
| A. | NaNO3、NaCl、KNO3、(NH4)2SO4 | B. | H2SO4、HCl、AgNO3、Na2SO4 | ||
| C. | KMnO4、CuCl2、Fe2(SO4)3、NaNO3 | D. | K2SO4、NaCl、K2CO3、NaOH |