题目内容
16.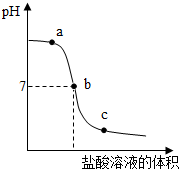 向氢氧化钠溶液中不断滴入盐酸,得到如图的曲线,下列有关判断不正确的是( )
向氢氧化钠溶液中不断滴入盐酸,得到如图的曲线,下列有关判断不正确的是( )| A. | a点时溶液中有氢氧化钠和氯化钠 | |
| B. | a点到b点溶液中盐酸的量不断增大 | |
| C. | b 点时,HCl 与NaOH恰好完全反应 | |
| D. | b 点到c点时,溶液中氯化钠的量不再增加 |
分析 根据盐酸显酸性,pH小于7,氢氧化钠显碱性,pH大于7;盐酸和氢氧化钠反应能生成氯化钠和水;盐酸和氢氧化钠完全反应时,溶液显中性进行分析解答.
解答 解:A、a点已经滴入一定量的盐酸,盐酸与氢氧化钠反应生成氯化钠,但溶液的pH值仍大于7,说明氢氧化钠还有剩余,故溶液中既有氢氧化钠又有氯化钠,故A说法正确;
B、b点溶液的pH值等于7,说明盐酸与氢氧化钠恰好完全反应,故从a点到b点溶液中滴入的盐酸完全和氢氧化钠反应,故溶液中没有盐酸,故B说法错误;
C、b点溶液的pH值等于7,说明盐酸与氢氧化钠恰好完全反应,故C说法正确;
D、b点溶液的pH值等于7,说明盐酸与氢氧化钠恰好完全反应,再滴入盐酸,由于氢氧化钠已消耗完全,故溶液中氯化钠的量不再增加,故D说法正确;
故选B.
点评 解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
6.下列物质含有氧气分子的是( )
| A. | 空气 | B. | 干冰 | C. | 二氧化锰 | D. | 高锰酸钾 |
1.有关空气及成分的说法正确的是( )
| A. | 空气是一种宝贵的自然资源 | |
| B. | 空气中氮气约占空气总体积的五分之一 | |
| C. | 空气中的稀有气体不与任何气体发生反应 | |
| D. | 汽车排放的尾气不会对空气造成污染 |
5.固态碘受热成紫红色的碘蒸气,无论是固态碘还是碘蒸气,都能使切开的土豆变成蓝色,这说明( )
| A. | 分子在不停运动 | B. | 分子间有间隔 | ||
| C. | 分子有一定大小 | D. | 同种分子性质相同 |