题目内容
12. A、B、C属于不同类别的化合物,分别和食盐含有一种相同元素,且它们发生的反应均属于复分解反应.“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,一种A与B反应有气体放出,请写出A、B、C的化学式:ANa2CO3;BHCl;CNaOH.
A、B、C属于不同类别的化合物,分别和食盐含有一种相同元素,且它们发生的反应均属于复分解反应.“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,一种A与B反应有气体放出,请写出A、B、C的化学式:ANa2CO3;BHCl;CNaOH.
分析 可以根据硫酸的化学性质进行分析,从而得出正确的结论;硫酸可以与某些金属单质、某些金属氧化物、碱、某些盐发生化学反应,且A、B、C属于不同类别的化合物,分别和食盐含有一种相同元素,据此分析.
解答 解:能和硫酸反应的物质类型有,某些金属单质(金属活动性顺序表中H前的金属)、某些金属氧化物、碱、某些盐,B是硫酸反应后的生成物,A、B、C属于不同类别的化合物,分别和食盐含有一种相同元素,其中A与B反应有气体放出,根据复分解反应的原理,可知是酸与碳酸盐的反应,A能够和硫酸反应,因此A可以是碳酸钠,则B是盐酸,C就是氢氧化钠,带入验证符合转化关系;故填:Na2CO3;HCl;NaOH.
点评 解答此题的关键是掌握硫酸的化学性质,要求同学们在平时的学习过程中,要掌握重要物质的性质,才能准确解答.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
3.下列化学实验基本操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
7.下列说法中不正确的是( )
| A. | 把铅加入锡中制成合金焊锡,主要目的是降低焊锡的熔点 | |
| B. | 衣料中的棉、羊毛等都属于合成有机高分子材料 | |
| C. | 活性炭能净化水是因为有吸附作用 | |
| D. | 洗涤剂能清洗油污,因为它有乳化作用 |
17. 经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
(1)下列说法中不正确的是B.
A、酸和碱中一定都含有氢元素
B、氯化钠由氯化钠离子构成
C、多数酸和碱都有腐蚀性
D、浓硫酸可用作某些气体的干燥剂
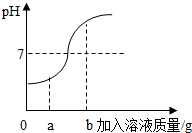
(2)在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示,该图横坐标代表的是NaOH溶液的质量.当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为(写化学式)NaCl.
(3)某敞口放置的氢氧化钠溶液已经变质,请用化学方程式表示其变质的原因.
(4)为了证明该瓶氢氧化钠溶液未完全变质,进行了以下实验,请将如表填写完整.
(5)现有部分变质的氢氧化钠样品18.6g与146g溶质质量分数为10%的盐酸溶液恰好完全反应生成CO24.4g,计算样品中NaOH的质量分数?
 经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.
经过一年的学习,我们对“酸碱盐”有了一定的认识,请回答下列有关问题.(1)下列说法中不正确的是B.
A、酸和碱中一定都含有氢元素
B、氯化钠由氯化钠离子构成
C、多数酸和碱都有腐蚀性
D、浓硫酸可用作某些气体的干燥剂
(2)在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示,该图横坐标代表的是NaOH溶液的质量.当加入该溶液的质量为ag时,所得溶液中含量最多的溶质为(写化学式)NaCl.
(3)某敞口放置的氢氧化钠溶液已经变质,请用化学方程式表示其变质的原因.
(4)为了证明该瓶氢氧化钠溶液未完全变质,进行了以下实验,请将如表填写完整.
| 实验操作 | 现象 | 结论或化学方程式 |
| 取少量该样品,滴加足量的BaCl2溶液,过滤 | 有白色沉淀生成 | 方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 在滤液中滴加酚酞溶液 | 滤液显红色 | 样品未完全变质 |
4.下列叙述错误的是( )
| A. | 蛋白质、糖类都属于有机物 | B. | 误食重金属盐可喝鲜牛奶解毒 | ||
| C. | 钛合金、玻璃钢都属于复合材料 | D. | 油脂由C、H、O三种元素组成 |
1.在一定条件下,甲和乙反应生成丙和丁,其反应的微观示意图如下所示:
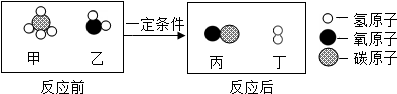
下列对该反应的叙述不正确的是( )

下列对该反应的叙述不正确的是( )
| A. | 反应前后原子个数不变 | |
| B. | 乙、丙都属于氧化物 | |
| C. | 生成的丙和丁的分子个数比为1:3 | |
| D. | 若将16g的甲和20g的乙混合反应,则生成丙和丁的质量之和一定为36g |
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子)请回答下列问题:
”表示氢原子)请回答下列问题: