题目内容
化学促进人类社会发展。
⑴ 可用Mg、Al等和稀硫酸反应制取氢气,反应类型属于__________反应;也可用Mg、Al和NaOH溶液组成化学电池,它可以将化学能转化为_________能。
⑵ Mg17Al12是一种新型储氢材料,一定条件下完全吸氢后转化为MgH2和Al,反应方程式为_____。
⑶ 科学家认为“氢能将成为未来的理想能源”,原因是(___________)
A.完全燃烧放出热量多 B.制取原料资源不受限制
C.燃烧产物不污染环境 D.目前制取效率高成本低
置换 电 Mg17Al12+17H2 17MgH2+12Al ABC 【解析】⑴ 可用Mg、Al等和稀硫酸反应制取氢气,反应类型属于置换反应,一种单质和一种化合物反应生成另一种单质和另一种化合物;也可用Mg、Al和NaOH溶液组成化学电池,它可以将化学能转化为电能。⑵ Mg17Al12是一种新型储氢材料,一定条件下完全吸氢后转化为MgH2和Al,反应方程式为Mg17Al12+17H2 ...
练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列实验操作中(括号内为杂质或待检验物质)不能达到实验目的是
选项 | 物质 | 目的 | 主要实验操作 |
A | 米粉、奶粉 | 鉴别 | 取样,灼烧,闻气味 |
B | Na2CO3(NaOH)溶液 | 检验 | 滴加酚酞试液,观察溶液颜色变化 |
C | CaO(CaCO3)固体 | 除杂 | 高温煅烧至固体质量不变 |
D | MnO2、KCl固体 | 分离 | 溶解、过滤、洗涤、干燥、蒸发 |
A. A B. B C. C D. D
B 【解析】 选项 物质 目的 主要实验操作 A 米粉、奶粉 鉴别 奶粉主要含有蛋白质,米粉主要含有淀粉,取样,灼烧,闻气味,奶粉有烧焦羽毛气味,故A正确; B Na2CO3(NaOH)溶液 检验 滴加酚酞试液,碳酸钠溶液和氢氧化钠溶液均呈碱性,滴加酚酞试液均变红,无法通过观察溶液颜色变化检验,故A错误; C ...

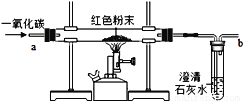


 B.
B. 
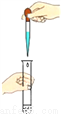 D.
D. 