题目内容
11.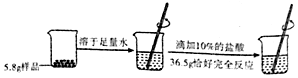 某混合物中含有氯化钠和碳酸钠,为测定碳酸钠的质量分数,小明进行了如图实验,请计算:
某混合物中含有氯化钠和碳酸钠,为测定碳酸钠的质量分数,小明进行了如图实验,请计算:(1)所用36.5g10%盐酸中溶质的质量;
(2)样品中碳酸钠的质量分数.
分析 (1)根据溶质的质量分数计算公式计算;
(2)根据碳酸钠与盐酸反应的方程式由盐酸中溶质的质量可求出碳酸钠的质量,即可求出样品中碳酸钠的质量分数.
解答 解:(1)所用36.5g10%盐酸中溶质的质量是:36.5g×10%=3.65g;
(2)设5.8g样品中碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 73
x 3.65g
$\frac{106}{73}=\frac{x}{3.65g}$ 解得x=5.3g
样品中碳酸钠的质量分数是:$\frac{5.3g}{5.8g}×100%$≈91.4%
答:(1)所用36.5g10%盐酸中溶质的质量是3.65g;(2)样品中碳酸钠的质量分数是91.4%.
点评 本题考查了氯化钠与碳酸钠的化学性质,同时考查了化学方程式的书写以及根据化学方程式计算溶液的质量分数,要求学生熟练掌握常见物质的化学性质以及相关的化学方程式.

练习册系列答案
相关题目
7.下列各组物质的溶液,根据它们自身的性质和相互间的反应现象,不用其它试剂就可以加以鉴别的是( )
| A. | FeCl3 NaCl Ba(OH)2 | B. | KCl HCl NNO3 | ||
| C. | Na2SO4 HCl H2SO4 | D. | CuCl2 NaNO3 K2SO4 |
19. 如图是氯化钾的溶解度曲线,下列说法错误的是( )
如图是氯化钾的溶解度曲线,下列说法错误的是( )
 如图是氯化钾的溶解度曲线,下列说法错误的是( )
如图是氯化钾的溶解度曲线,下列说法错误的是( )| A. | t1℃时,氯化钾的溶解度是31g | |
| B. | 氯化钾在热水中的溶解度比在冷水中的大 | |
| C. | 通过降低温度,可将氯化钾的不饱和溶液变为饱和溶液 | |
| D. | t2℃时,氯化钾饱和溶液中溶质的质量分数为40% |
3.2016年12月22日,我国首颗全球二氧化碳监测科学实验卫星发射升空,填补了我国在温室气体监测方面的技术空白,下列有关CO2的说法中正确的是( )
| A. | 其能与血红蛋白结合而使人中毒 | B. | 碳元素与氧元素的质量比是1:2 | ||
| C. | 由一个碳原子和一个氧分子构成 | D. | 碳元素的化合价为+4 |
 人体通过肺与外界进行气体交换,为了探究人在呼吸过程中所呼出气体中的二氧化碳气体究竟是空气中原有的,还是人体代谢时所产生的,我们可以采用了右图所示的装置进行实验(锥形瓶中盛有足量的石灰水).
人体通过肺与外界进行气体交换,为了探究人在呼吸过程中所呼出气体中的二氧化碳气体究竟是空气中原有的,还是人体代谢时所产生的,我们可以采用了右图所示的装置进行实验(锥形瓶中盛有足量的石灰水).
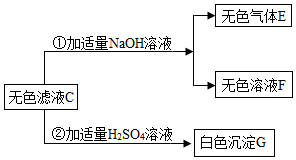 已知某固体混合物A中可能含有CuSO4、NH4Cl、NaNO3、Ba(NO3)2、CaCO3、Na2CO3六种物质中的两种或多种,按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所发生的反应都恰好完全反应).
已知某固体混合物A中可能含有CuSO4、NH4Cl、NaNO3、Ba(NO3)2、CaCO3、Na2CO3六种物质中的两种或多种,按下述步骤进行实验探究,观察实验现象,并加以分析推理(设过程中所发生的反应都恰好完全反应).

