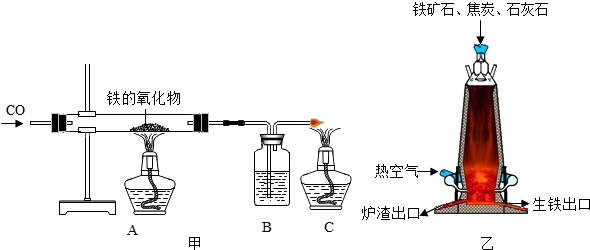
题目内容
4.如图是一些物质的转化关系图,其中E是一种红色固体,F是单质,乙在常温下是一种液体,丙是一种有毒气体,G的溶液呈黄色,部分反应条件已略去.请回答: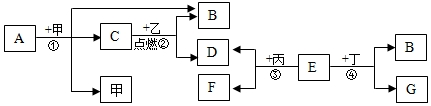
(1)甲在反应中所起的作用是催化作用.
(2)反应②的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,反应③的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)反应④在生产、生活中的应用是除铁锈.
分析 根据G的溶液呈黄色,所以G中含有铁离子,E是一种红色固体,和丙反应会生成单质F和D,丙是一种有毒气体,所以丙就是一氧化碳,E就是氧化铁,F就是铁,D就是二氧化碳,所以丁是酸,B就是水,A会生成水和C,C和乙又会生成水和二氧化碳,所以A就是双氧水,C就是氧气,乙就是含有碳氢元素的有机物,
根据甲在反应前后的变化进行分析,根据(1)中推出的反应物、生成物书写方程式,根据推出的反应④分析用途.
解答 解:G的溶液呈黄色,所以G中含有铁离子,E是一种金属氧化物,和丙反应会生成单质F和D,丙是一种有毒气体,所以丙就是一氧化碳,E就是氧化铁,F就是铁,D就是二氧化碳,所以丁是酸,B就是水,A会生成水和C,C和乙又会生成水和二氧化碳,所以A就是双氧水,C就是氧气,乙就是含有碳氢元素的有机物,
甲在反应前后没有发生变化,所以甲是催化剂,
乙可能是甲烷,甲烷燃烧生成二氧化碳和水;一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳;
酸会与金属氧化物反应,可以除去铁表面的铁锈,
故答案为:(1)催化作用;
(2)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)除铁锈.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
相关题目
9.下列物质的用途主要利用物质的物理性质的是( )
| A. | 碳酸氢钠用于治疗胃酸过多 | B. | 干冰用作人工降雨 | ||
| C. | 盐酸用于除铁锈 | D. | 熟石灰用于改良酸性土壤 |
13.物理变化与化学变化的根本区别是( )
| A. | 颜色是否发生了变化 | B. | 物质的状态是否发生了变化 | ||
| C. | 物质的种类是否发生了变化 | D. | 物质的质量是否发生了变化 |
14.化学实验有助于理解化学知识,形成化学观念,提升科学素.用如图所示装置进行实验(夹持装置已省略).请完成下列内容.
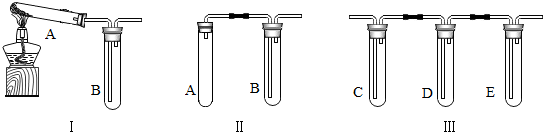
(1)制取气体.
(2)证明二氧碳能与水反应,将制CO2的装置与Ⅲ装置连接,若B中装入饱和NaHCO3溶液,则C、D、E中还应分别装入硝酸银溶液、浓硫酸、紫色石蕊试液.
(3)探究碳的还原性,将图中的Ⅰ、Ⅲ装置连接,在Ⅰ装置的A试管中加入碳和氧化铜粉末.若反应既有CO2又有CO生成,要证明CO2生成并收集CO,B、D中都加入澄清石灰水,C中加入NaOH溶液,证明有CO2生成的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,D的作用是检验二氧化碳是否被C中的氢氧化钠溶液完全吸收,E用于收集CO,应对E装置进行的调整是进气管短,出气管要长.

(1)制取气体.
| 气体 | 反应物 | 装置 | 化学方程式 |
| O2 | Ⅰ | ||
| CO2 | 石灰石、稀盐酸 |
(3)探究碳的还原性,将图中的Ⅰ、Ⅲ装置连接,在Ⅰ装置的A试管中加入碳和氧化铜粉末.若反应既有CO2又有CO生成,要证明CO2生成并收集CO,B、D中都加入澄清石灰水,C中加入NaOH溶液,证明有CO2生成的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,D的作用是检验二氧化碳是否被C中的氢氧化钠溶液完全吸收,E用于收集CO,应对E装置进行的调整是进气管短,出气管要长.

 新药帕拉米韦注射液可用于治疗H7N9禽流感.其说明书中部分如图.
新药帕拉米韦注射液可用于治疗H7N9禽流感.其说明书中部分如图.