题目内容
14.水的状态除了气、液和固态外,还有玻璃态.它是由液态水急速冷却到l65K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )| A. | 同温度同质量液态水和玻璃态水,体积相同 | |
| B. | 玻璃态水不属于氧化物 | |
| C. | 玻璃态水和普通水的化学性质相同 | |
| D. | 玻璃态水分子不运动 |
分析 A、根据玻璃态水与液态水密度的关系考虑.
B、根据水的组成结构及氧化物质的定义判断.
C、根据玻璃态水与普通水的成分分析.
D、玻璃态的水中的水分子具有微观粒子的性质,分子是不断运动的.
解答 解:A、由玻璃态的水密度与普通液态水的密度相同,所以同温度同质量液态水和玻璃态水,体积相同,故正确;
B、氧化物是指由两种元素组成,并且其中一种为氧元素的化合物,而玻璃态的水是由氢氧两种元素组成的化合物,所以错误;
C、玻璃态水与普通水的成分一样,所以化学性质相同,所以正确;
D、玻璃态的水中的水分子具有微观粒子的性质,分子是不断运动的,故C错误.
故选AC.
点评 物质的分类是重点的基础化学知识,但却是学习难点之一,要能正确地、合理地对物质作出正确分类,首先要理解物质分类的有关概念,抓住概念间的相互关系和本质区别.

练习册系列答案
相关题目
6.要除去二氧化碳中混有的一氧化碳,可把混合气体通过( )
| A. | 在足量的氧气中燃烧 | B. | 炽热的炭层 | ||
| C. | 澄清石灰水 | D. | 灼热的氧化铜 |
2.现甲、乙两化学小组安装两套如图1所示相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
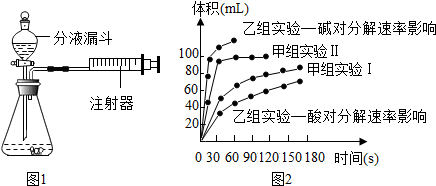
(1)下列方法不能检查该装置气密性的是C.
A.将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B.关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C.关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)甲小组有如下实验设计方案,完成下表.
(3)甲、乙两小组得出如图2数据.
①由甲组实验得出的数据可知:浓度越大,H2O2分解速率越快.
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;乙组提出可以用Ba02固体与硫酸溶液反应制H202(已知还生成另一种物质),其化学反应方程式为BaO2+H2SO4=BaSO4↓+H2O2;支持这一方案的理由是过氧化氢在酸性环境下分解较慢.

(1)下列方法不能检查该装置气密性的是C.
A.将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B.关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C.关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)甲小组有如下实验设计方案,完成下表.
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2% H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5% H2O2 |
①由甲组实验得出的数据可知:浓度越大,H2O2分解速率越快.
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;乙组提出可以用Ba02固体与硫酸溶液反应制H202(已知还生成另一种物质),其化学反应方程式为BaO2+H2SO4=BaSO4↓+H2O2;支持这一方案的理由是过氧化氢在酸性环境下分解较慢.
9.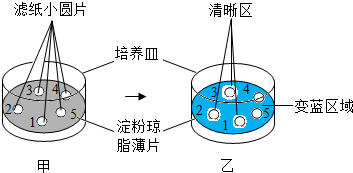 某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:
某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:
①取5片大小相同的滤纸小圆片,编为1-5号,将其分别在五种不同的成分的溶液(各溶液成分如表)中浸泡后取出,按如图甲所示放置在盛有淀粉琼脂薄片的培养皿中,盖上盖子.
②将培养皿置于37℃的恒温箱中国,半小时后取出,将碘液均匀滴入培养皿中,约1分钟后用清水缓缓冲去多余的碘液.
③实验结果发现:1号、2号和3号滤纸小圆片周围出现了大小不等的清晰区(即没有变蓝色的区域),其中3号周围的清晰区面积最大,4号和5号周围以及其余部位均显蓝色,如图乙所示.
(1)为什么1号、2号和3号滤纸小圆片周围会出现清晰区?因为1-3号小圆片上有淀粉酶,淀粉在淀粉酶的催化作用下分解了.
(2)为了判断酸性对该淀粉酶催化作用的影响,应选择第2号与哪几号进行对照?1和4.(填滤纸编号).
(3)实验结果表明,弱碱性(选填“弱酸性”、“中性”或“弱碱性”)条件下,该淀粉酶的催化作用最强.
 某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:
某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:①取5片大小相同的滤纸小圆片,编为1-5号,将其分别在五种不同的成分的溶液(各溶液成分如表)中浸泡后取出,按如图甲所示放置在盛有淀粉琼脂薄片的培养皿中,盖上盖子.
②将培养皿置于37℃的恒温箱中国,半小时后取出,将碘液均匀滴入培养皿中,约1分钟后用清水缓缓冲去多余的碘液.
③实验结果发现:1号、2号和3号滤纸小圆片周围出现了大小不等的清晰区(即没有变蓝色的区域),其中3号周围的清晰区面积最大,4号和5号周围以及其余部位均显蓝色,如图乙所示.
| 滤纸编号 | 溶液成分 |
| 1 | 淀粉酶溶液 |
| 2 | 淀粉酶溶液-稀盐酸 |
| 3 | 淀粉酶溶液-稀碳酸钠溶液 |
| 4 | 稀盐酸 |
| 5 | 稀碳酸钠溶液 |
(2)为了判断酸性对该淀粉酶催化作用的影响,应选择第2号与哪几号进行对照?1和4.(填滤纸编号).
(3)实验结果表明,弱碱性(选填“弱酸性”、“中性”或“弱碱性”)条件下,该淀粉酶的催化作用最强.
19.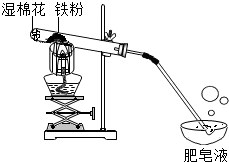 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑.
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
【拓展】把赤铁矿冶炼成铁,其主要反应原理是在高温下,一氧化碳夺取铁矿石里的氧,将铁还原出来,请写出化学反应方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
【拓展】把赤铁矿冶炼成铁,其主要反应原理是在高温下,一氧化碳夺取铁矿石里的氧,将铁还原出来,请写出化学反应方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
3.除去下列各组物质中的少量杂质,所用方法不可行的是( )
| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | MnO2 | 炭粉 | 在空气中灼烧 |
| B | CO2 | CO | 点燃 |
| C | FeSO4 | CuSO4 | 加入足量铁屑,充分反应后过滤 |
| D | CaO | CaCO3 | 高温 |
| A. | A | B. | B | C. | C | D. | D |
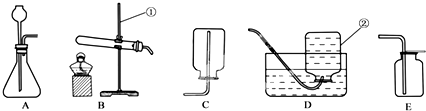
 B.
B. 
 D.
D. 