题目内容
某混合气体可能含有CO、H2、和H2O(气)中的一种或几种,为验证其组成,同学们进行实验的装置和现象如下(夹持仪器已省略,假设气体均吸收完全).
【查阅自来哦】:污水硫酸铜是白色粉末,遇水变为蓝色.

(1)A装置的作用 ;B装置的作用 .
(2)装置D中溶液变浑浊的化学方程式是 .点燃尾气,火焰呈 色.
(3)丁认为,由于他们对装置 (填序号)中的实验现象分析不同而导致结论有差异.根据碳酸盐可转化为CO2的性质,丁利用上述实验结束后装置内药品和某种常见试剂进行实验,证明了甲的结论是正确的.请写出丁的实验操作过程与现象 .
【查阅自来哦】:污水硫酸铜是白色粉末,遇水变为蓝色.

| 结论 | 甲 | 乙 | 丙 |
| 含有CO、H2、H2O(气) | 含有CO、H2、CO2 | 含有CO、H2、CO2、H2O(气) |
(2)装置D中溶液变浑浊的化学方程式是
(3)丁认为,由于他们对装置
考点:常见气体的检验与除杂方法,书写化学方程式、文字表达式、电离方程式
专题:物质的检验、鉴别与推断
分析:由题意可知,按照实验步骤依次进行实验.①氢氧化钠固体具有吸水性和吸收二氧化碳性,氢氧化钠固体质量增加,说明气体中有水蒸气或二氧化碳?②灼热的氧化铜,黑色粉末变红色,说明有一氧化碳或氢气或二者的混合气体?③无水硫酸铜,白色粉末变蓝,说明上一步反应生成了水,有氢气?④澄清的石灰水,石灰水变浑浊,说明②的反应中有二氧化碳气体生成,同时说明混合气体中有CO.
解答:解:(1)氢氧化钠固体具有吸水性和吸收二氧化碳性,所以A装置的作用是吸收水分和二氧化碳;一氧化碳和氢气能够还原氧化铜,使黑色粉末变红色,所以B装置的作用是验证是否有氢气和一氧化碳.
故答案是:是验证是否有水分和二氧化碳;验证是否有氢气和一氧化碳.
(2)CO2能使澄清石灰水变浑浊,因为二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,其反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
由A得出结论是有水蒸气或二氧化碳;由B得出结论是有一氧化碳或氢气,或二者的混合气体;由C得出的结论是一定有还原性气体氢气;由D得出的结论是还原性气体一氧化碳.
所以,尾气中含有CO、H2,CO、H2和O2燃烧时发出蓝色.
故答案是:CO2+Ca(OH)2═CaCO3↓+H2O;蓝;
(3)若混合气体中含有CO2、H2O(气),则在A中的氢氧化钠会吸收二氧化碳而成为碳酸钠,所以利用稀盐酸进行验证即可.若加入稀盐酸后,有气泡冒出,则氢氧化钠吸收了二氧化碳气体,若无现象发生,则原混合气体中无二氧化碳气体;
故答案是:A;将A中固体取出,加入烧杯(试管)中,加入过量稀盐酸,无明显现象.
故答案是:是验证是否有水分和二氧化碳;验证是否有氢气和一氧化碳.
(2)CO2能使澄清石灰水变浑浊,因为二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,其反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
由A得出结论是有水蒸气或二氧化碳;由B得出结论是有一氧化碳或氢气,或二者的混合气体;由C得出的结论是一定有还原性气体氢气;由D得出的结论是还原性气体一氧化碳.
所以,尾气中含有CO、H2,CO、H2和O2燃烧时发出蓝色.
故答案是:CO2+Ca(OH)2═CaCO3↓+H2O;蓝;
(3)若混合气体中含有CO2、H2O(气),则在A中的氢氧化钠会吸收二氧化碳而成为碳酸钠,所以利用稀盐酸进行验证即可.若加入稀盐酸后,有气泡冒出,则氢氧化钠吸收了二氧化碳气体,若无现象发生,则原混合气体中无二氧化碳气体;
故答案是:A;将A中固体取出,加入烧杯(试管)中,加入过量稀盐酸,无明显现象.
点评:该题是实验推断题,在熟练掌握各气体性质的基础上,主要考查分析推理能力.关键是严谨全面.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
下列关于燃烧的现象的描述,正确的是( )
| A、氢气在氧气中燃烧产生大量的白烟 |
| B、铁丝在空气中剧烈燃烧,火星四射 |
| C、红磷在空气中燃烧发出耀眼的白光 |
| D、硫在氧气中燃烧会发出蓝紫色火焰 |

 如图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物.胃液中含有适量的甲,可帮助消化,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物,生成物略去.
如图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物.胃液中含有适量的甲,可帮助消化,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物,生成物略去.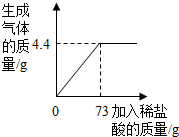 某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图.
某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图.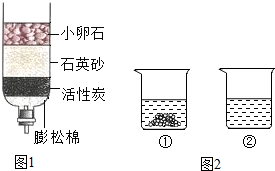 水和溶液在生活中起着十分重要的作用.
水和溶液在生活中起着十分重要的作用.